已知七种短周期元素a~g的有关信息如下表所示:
| 元素编号 | a | b | c | d | e | f | g |
| 原子半径 / nm | 0.037 | 0.074 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低化合价 | +1 | -2 | +3 | -2 | +3 | +1 | +1 |
下列推断正确的是
A.简单离子的离子半径:g < e
B.氢化物的稳定性强弱:b > d
C.元素e的氧化物是两性氧化物
D.元素a与元素d形成的化合物属于离子化合物
下图为短周期的一部分,Y原子最外层电子数是其电子层数的2倍,下列说法正确的是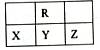
| A.Y的氢化物比Z的氢化物稳定 |
| B.原子半径大小顺序是X >Y>R |
| C.Y、R形成的化台物YR2能使酸性KMnO4溶液褪色 |
| D.四种元素中最高价氧化物的水化物的酸性最强的是Y |
X、Y、Z、W均为短周期元素,在周期表中位置如图,Y原子的最外层电子数是其次外层电子数的3倍。下列说法正确的是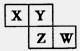
| A.X、Y、Z的原子半径大小:X>Y>Z |
| B.X、W的气态氢化物能相互反应,生成共价化合物 |
| C.Z、W的最高价氧化物对应水化物的酸性,前者更强 |
| D.Y的单质与氢气反应较Z剧烈 |
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是
| A.原子序数:W>Z>X |
| B.气态氢化物的稳定性:N>R |
| C.Y和W形成共价化合物 |
| D.X和Z两者最高价氧化物对应的水化物能相互反应 |
下图是部分短周期主族元素原子半径与原子序数的关系图。则下列说法正确的是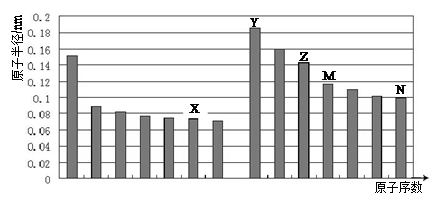
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH﹤Ba(OH)2 |
X、Y、Z三种短周期非金属元素在元素周期表中的位置如图所示,下列说法正确的是
| X | | Y |
| | | Z |
A.原子的半径:Y大于X
B.氢化物的稳定性:X大于Y
C.最高价氧化物水化物的酸性:Z强于Y
D.Z原子比Y原子多一个电子层
短周期元素A、B、C、D在元素周期表中的相对位置如图所示,其中B所处的周期序数与族序数相等。下列判断不正确的是
| | | A | |
| B | C | | D |
A.最简单气态氢化物的热稳定性:A>C
B.最高价氧化物对应水化物的酸性:C<D
C.原子半径:B>C>A
D.含B元素的盐溶液一定显酸性
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是
| | Q | R | |
| T | | | W |
A.T的氧化物是光导纤维的主要成分
B.W的氢化物的化学式为HCl
C.R的最高正价氧化物的水化物是弱电解质
D.Q与氢形成的化合物均含极性共价键
