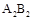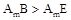下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是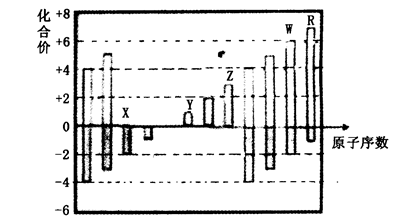
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R<W |
| C.WX3和水反应生成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
X、Y、Z是3种短周期元素,其中X、Y位于同一主族,Y、Z位于同一周期,X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原予少1。下列说法不正确的是
| A.三种元素的非金属性由弱到强的顺序为Z<Y<X |
| B.Y元素的最高价氧化物对应水化物的化学式可表示为H2YO4 |
| C.3种元素的气态氧化物中.Z的气态氢化物最稳定 |
| D.原子半径由大到小排列顺序为Z>Y>X |
可能存在的第119号未知元素,有人称为“类钫”,根据元素周期表结构及性质变化趋势,判断有关“类钫”的预测正确的是
| A.具有放射性 | B.单质有较高的熔点 |
| C.在化合物中呈+2价 | D.单质的密度小于1 g/cm3 |
下表是元素周期表的一部分,请根据表中a~k对应元素,回答下列有关问题:
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | | a | | b | |
| 3 | c | d | e | f | | g | h | |
| 4 | J | | | | | | k | |
(1)写出a的原子的最外层电子排布式 ,a的原子最外层有 个未成对电子。
(1)在上述元素中的最高价氧化物对应的水化物中,最强酸的化学式是 ;最强碱与两性氢氧化物反应的化学方程式为: 。
(1)写出上述元素中和Ar核外电子排布相同的离子半径由大到小的顺序: (用离子符号表示),上述两种元素能结合成XY型离子化合物,且每个阴、阳离子中均含10个电子,已知常温下该物质的水溶液显碱性,其原因是 (用离子方程式表示)。
(1)下列能用作f和g元素非金属性强弱比较的判断依据的是( )
A.单质熔点:
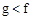
B.最高价氧化物对应水化物的酸性:
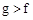
C.最高价氧化物对应水化物的溶解性:
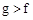
D.f不能与氢气反应,g能与氢气反应
已知元素周期表前三周期元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,
下列关系正确的是
| A.质子数c>b | B.离子还原性Y2->Z- |
| C.氢化物稳定性H2Y>HZ | D.原子半径X<W |
月球上的每百吨He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元素主要以He的形式存在。已知一个12C原子的质量为a g,一个He原子的质量为b g,NA为阿伏加德罗常数。下列说法正确的是
| A.He比H多一个中子 | B.氦元素的近似相对原子质量为3 |
| C.He的相对原子质量为12b/a | D.He的摩尔质量为bNA |
下列说法不正确的是( )
| A.NH4+中质子数和电子数相等 |
| B.乙醇比乙二醇的沸点低 |
| C.乙炔与苯的实验式均为CH |
| D.过氧化钠与过氧化氢中均含有非极性键 |
依据元素周期表及元素周期律,下列推断正确的是
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.ⅠA族元素的金属性比ⅡA族元素的金属性强 |
| C.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
| D.主族元素的最高正化合价等于该元素原子的最外层电子数 |