题目内容
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是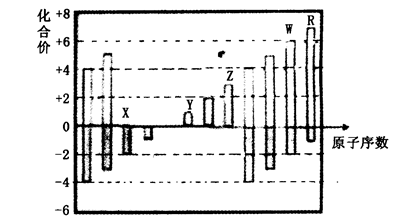
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:R<W |
| C.WX3和水反应生成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
D
解析试题分析:由表中化合价可知,X的化合价为-2价,没有正化合价,故X为O元素。Y的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素。Z为+3价,为Al元素。W的化合价为+6、-2价,故W为S元素,R的化合价为+7、-1价,故R为Cl元素。则A、X、Y、Z、W、R分别为O、Na、Al、S、Cl,同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,因此原子半径的顺序应为Y>Z>W>R>X,故A错误;B、非金属性越强,氢化物的稳定性越强。非金属性Cl>S,故氢化物稳定性HCl>H2S,故B不正确;C、SO3和水反应生成硫酸,硫酸是共价化合物,C不正确;D、Al(OH)3具有两性,可与NaOH溶液反应生成偏铝酸钠和水,故D正确,答案选D。
考点:考查元素周期律应用、化学键、化合物判断以及氢氧化铝性质等

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
五种短周期元素X、Y、Z、M、N的原子序数依次增大,X、Y、Z、M是组成蛋白质的基础元素,M原子的最外层电子数是电子层数的3倍,N2M2可用于潜水艇中作为氧气的来源,下列说法错误的是
| A.与Y同主族的短周期元素可与强碱反应生成氢气 |
| B.X和M形成的化合物分子中可能含有非极性共价键 |
| C.由X、Z、M形成的化合物一定是共价化合物 |
| D.等物质的量的N2YM3粉末和NXYM3粉末分别与等浓度的盐酸反应,后者反应速率要快 |
现有下列短周期元素性质的数据:
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | | +2 | +1 | +5 | +7 | +1 | +5 | +3 |
| -2 | | | -3 | -1 | | -3 | |
下列说法正确的是
A.原子序数④元素大于⑦元素
B.②.③处于同一周期
C.上述八种元素最高价氧化物对应的水化物,⑤号酸性最强
D.⑧号元素原子结构示意图为:

短周期元素X、Y的原子序数相差6,下列有关判断错误的是
| A.X与Y可能位于同一周期或相邻周期 |
| B.X与Y可能位于同一主族或相邻主族 |
| C.X与Y可能形成离子晶体XY |
| D.X与Y可能形成原子晶体YX2 |
月球上的每百吨He聚变所释放出的能量相当于目前人类一年消耗的能量,地球上氦元素主要以He的形式存在。已知一个12C原子的质量为a g,一个He原子的质量为b g,NA为阿伏加德罗常数。下列说法正确的是
| A.He比H多一个中子 | B.氦元素的近似相对原子质量为3 |
| C.He的相对原子质量为12b/a | D.He的摩尔质量为bNA |
X、Y、Z、W是原子序数依次增大的短周期主族元素,X与Z同主族,X原子的最外层电子数是其最内层电子数的2倍,Y原子的最外层电子数比W原子的少2个。下列叙述一定正确的是
| A.X、Y的单质均可以导电 |
| B.原子半径:Z>W |
| C.X、Z的氧化物均为酸性氧化物 |
| D.Y、W的最高价氧化物的水化物均易溶于水 |
