如图是两个氢原子相互接近时的能量变化图,则有关该图的说法正确的是( )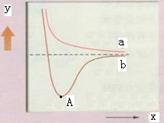
| A.y代表两原子之间的核间距 |
| B.x代表体系具有的能量 |
| C.a代表核外电子自旋相反的两个氢原子能量变化 |
| D.A点时表示两原子间形成了稳定的共价键 |
下列关于d轨道的说法错误的是( )
| A.M层才开始出现d轨道 |
| B.d轨道最早出现在第4周期元素 |
| C.电子排布时,3d轨道能量高于4s轨道 |
| D.d轨道有10种空间伸展方向 |
短周期元素X、Y、W、Q在元素周期表中的相对位置如下图所示。常温下,Al能溶于W 的最髙价氧化物的水化物的稀溶液,却不溶于其浓溶液。下列说法正确的是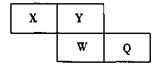
| A.Y的最髙化合价为+6 |
| B.离子半径:W>Q>Y>X |
| C.氢化物的沸点:Y>Q |
| D.最髙价氧化物的水化物的酸性:W>Q |
已知短周期元素甲、乙、丙、丁、戊的原子序数依次增大,它们的部分化合价如下表。下列说法正确的是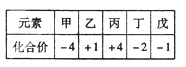
| A.乙的单质中能与水剧烈反应 |
| B.气态氢化物的稳定性:丙>甲 |
| C.丙的氧化物能与戊的氢化物水溶液反应 |
| D.其最高价氧化物对应的水化物的酸性:丁>戊 |
短周期主族元素X、Y、Z在元素周期表中的相对位置如图,下列推论合理的是
| X | Y |
| | Z |
A.若Y和Z能形成化合物,则X为氮元素
B.若X、Y、Z的单质常温下都是气体,则Y为氧元素
C.若X、Y、Z是非金属元素,则它们气态氢化物的水溶液都显酸性
D.若X、Y、Z的原子序数之和小于20,则它们都是金属元素
短周期元素W、X、Y和Z的原子序数依次增大,元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法错误的是
| A.元素W、X的氯化物中,各微粒均满足8电子的稳定结构 |
| B.元素X与氢形成的电子比为1:1的化合物有很多种 |
| C.元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 |
| D.元素Z可与元素X形成共价化合物XZ2 |
下列有关比较中,大小顺序排列不正确的是
| A.第一电离能:O>N>C |
| B.酸性强弱:HNO3>H2CO3>HClO |
| C.氢化物热稳定性:NH3>PH3>SiH4 |
| D.原子半径大小顺序:r (Mg)>r (Al)>r (N) |
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | 啤酒和饮料中常溶有X的最高价氧化物,打开瓶子时,这种氧化物会大量逸出 |
| Y | Y2是空气中含量最高的气体单质 |
| Z | Z的基态原子最外层电子排布式为2s22p4 |
| W | W的一种核素质量数为27,中子数为14 |
(1)W位于元素周期表第 周期第 族;Z和W的最简单的离子半径大小关系为
(用离子符号表示)
(2)一种X形成的单质,是自然界硬度最大的物质,若熔化这种单质,所需克服的微粒间的作用力是 ;Y的电负性比Z (填“大”或“小”)
(3)W的单质与NaOH溶液反应的离子方程式为 , W在高温条件下可还原高熔点的金属氧化物制的金属单质,写出W还原Cr2O3反应的化学方程式: 。
(4)煤燃烧产生的烟气中有Y的氧化物,会引起严重的环境问题,因此,常用XH4催化还原以消除污染,已知:
XH4(g)+2 YO2(g)="=" Y2(g)+ XO2(g)+2H2O (g) △H1= -867kJ/mol
2 YO2(g)
 Y2O4(g) △H2=-56.9kJ/mol
Y2O4(g) △H2=-56.9kJ/mol 工业上常利用液晶显示屏生产过程中产生的废玻璃粉末为原料回收金属铈(Ce),金属铈是一种重要的稀土元素,原子序数为58,它有四种同位素,元素的相对原子质量为140,下列有关说法正确的是
| A.它是第五周期元素 |
| B.原子核内一定有82个中子 |
| C.铈的四种同位素形成的中性原子核外电子数相同 |
| D.Ce2+离子中有55个质子 |