题目内容
如图是两个氢原子相互接近时的能量变化图,则有关该图的说法正确的是( )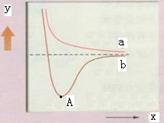
| A.y代表两原子之间的核间距 |
| B.x代表体系具有的能量 |
| C.a代表核外电子自旋相反的两个氢原子能量变化 |
| D.A点时表示两原子间形成了稳定的共价键 |
D
解析试题分析:A点能量最低,形成了稳定的共价键,D项正确;y代表体系的能量,A、B项错误;自旋相反的是电子,不是原子,C项错误。
考点:本题考查化学键的形成与能量的关系。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
以下有关原子结构及元素周期律的叙述正确的是
A. 是中子数不同质子数相同的同种核素 是中子数不同质子数相同的同种核素 |
| B.第IA族金属元素是同周期中金属性最强的元素 |
| C.第ⅦA族元素从上到下,其氢化物的稳定性逐渐增强 |
| D.短周期元素形成离子后,最外层都达到8电子稳定结构 |
下列说法正确的是
| A.原子最外层电子数为2的元素一定处于周期表IIA族 |
| B.原子序数相差2的两元素不可能处于同一主族 |
| C.可根据氢化物的稳定性和酸性强弱,来判断非金属元素得电子能力强弱 |
| D.非金属元素的最高化合价不超过其元素电子的最外层电子数 |
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述正确的是
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.152 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6、-2 | -1 | -1 |
B.气态氢化物的稳定性HG>HF>H2E
C.B2+、D3+、E2-、G-四种离子的核外电子排布相同
D.单质的活泼性顺序为:A>C>B>D
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如右图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强,下列说法正确的是
| A.化合物XZW既含离子键也含共价键 |
| B.对应气态氢化物的稳定性Y>Z |
| C.对应简单离子半径:X>W |
| D.Y的氧化物能与Z或X的最高价氧化物对应的水化物反应 |