下列物质与水反应最剧烈的是( )
| A.Rb | B.K | C.Na | D.Li |
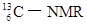 (核磁共振)可以用于含碳化合物的结构分析,有关
(核磁共振)可以用于含碳化合物的结构分析,有关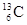 的说法正确的是( )
的说法正确的是( )
| A.质子数为6 | B.电子数为13 | C.中子数为6 | D.质量数为6 |
下列说法正确的是
A.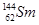 与 与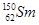 互为同位素 互为同位素 |
| B.氯气能使潮湿的蓝布条变为白色,说明氯气有漂白性 |
| C.将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L |
| D.焰色反应一定发生化学变化 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为14。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的2倍。下列说法不正确的是
| A.X的氢化物溶液与其最高价氧化物对应的水化物溶液的酸碱性相反 |
| B.Y的氧化物既可与强酸反应又可与强碱反应,并可用来制作耐火材料 |
| C.X和Z的最高价氧化物对应的水化物的浓溶液都是具有强氧化性的酸 |
| D.Z的氢化物比X的氢化物更稳定 |
如图所示为元素周期表的一部分,X、Y、W、Z均为短周期元素,其中只有X为金属元素。下列说法错误的是
| | W | Z |
| X | Y | |
A.原子半径:Z<W<Y<X
B.元素Y的氧化物能与NaOH溶液反应
C.最简单气态氢化物的热稳定性:Y>X
D.W、Z的氧化物都能与碱反应生成盐和水
下列说法正确的是
| A.电子层结构相同的微粒,其化学性质一定相似 |
| B.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| C.非金属元素的原子两两结合形成的化合物不一定是共价化合物 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
下列关于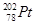 的说法正确的是
的说法正确的是
A.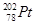 和 和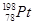 的质子数相同,互称为同位素 的质子数相同,互称为同位素 |
B.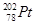 和 和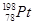 的中子数相同,互称为同位素 的中子数相同,互称为同位素 |
C.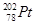 和 和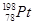 的核外电子数相同,是同一种核素 的核外电子数相同,是同一种核素 |
D.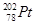 和 和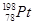 的质量数不同,不能互称为同位素 的质量数不同,不能互称为同位素 |
图中a、b、c、d、e、f为元素周期表中前4周期的一部分元素,下列有关叙述正确的是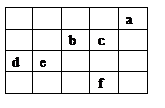
| A.b、c、e三种元素的原子半径大小关系:e>c>b |
| B.六种元素分别形成的单质固体中,d的熔、沸点最高 |
| C.c的氢化物沸点比f的氢化物沸点低 |
| D.b元素除0价外,只有一种化合价 |
下列顺序不正确的是
| A.热稳定性:HF>HCl>HBr>HI |
| B.微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C.电离程度(同温度同浓度溶液中):HCl>CH3COOH>NaHCO3 |
| D.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.071 | 0.099 |
| 主要化合价 | +2 | +3 | +6、-2 | -1 | -1 |
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4