短周期元素W、X、Y、Z的原子序数依次增大,且原子最外层电子数之和为14。W的原子半径比X的大,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最高的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
| A.元素X的最高价氧化物对应的水化物的酸性比Z的弱 |
| B.元素Y、Z的简单离子的电子层结构相同 |
| C.元素W与Z形成的化合物为共价化合物 |
| D.原子半径由大到小的顺序为:r(Z)>r(Y)>r (W) |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是
| A.原子半径:Z>W>R |
| B.对应的氢化物的热稳定性:R>W |
| C.W与X、W与Z形成的化合物的化学键类型完全相同 |
| D.Y的最高价氧化物对应的水化物是弱酸 |
下列各组顺序的排列不正确的是
| A.原子半径:Na>Mg>Al>H |
| B.热稳定性: HC l<H2S<PH3 |
| C.酸性强弱:H2SiO3<H2CO3<H3PO4 |
| D.氧化性:K+<Na+<Mg2+<Al3+ |
下列判断错误的是
A.沸点: |
B.熔点: |
C.酸性: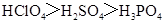 |
D.碱性: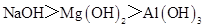 |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
下列说法正确的是
| A.离子键只存在于离子化合物中,共价键只存在于共价化合物中 |
| B.热稳定性:NH3>PH3>AsH3;酸性:HClO4>H2SO4>H3PO3 |
| C.BF3和CS2分子中所有原子的最外层都是8电子稳定结构 |
| D.钠离子的半径大于镁离子的半径,氯离子的还原性强于硫离子的还原性 |
四种短周期元素在周期表中的相对位置如右表所示,下列说法错误的是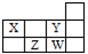
| A.X和Y元素的原子最外层电子数之和等于Z元素的原子最外层电子数的2倍 |
| B.Y元素的非金属性强于W元素的,其最高价氧化物水化物的酸性也强于W的 |
| C.X最简单氢化物溶于水呈碱性,Z最简单氢化物溶于水呈酸性 |
| D.W元素形成的单质可以从Z元素氢化物的水溶液中置换出Z单质 |
短周期主族元素X、Y、Z、W的原子序数依次增大,元素X的原子半径最小,Y元素和X元素在一定条件下能形成YX,Z和W的原子序数相差8,W原子的电子总数是其电子层数的5倍。下列叙述正确的是( )
| A.Y可用于制造高性能可充电电池 |
| B.WX3的沸点高于ZX3 |
| C.Z的最高价含氧酸的酸性强于W的最高价含氧酸的酸性 |
| D.原子半径的大小顺序:rW>rZ>rY>rX |
短周期元素W、X、Y、Z 的原子序数依次增大,W与Y最外层电子数之和为X的最外层电子数的2倍,Z最外层电子数等于最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是
| A.Y与Z的最高正价之和等于9 |
| B.Y的气态氢化物比W的稳定 |
| C.原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
| D.XY2与ZY2中的化学键类型相同 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知:
| W | X | |
| | Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性