题目内容
四种短周期元素在周期表中的相对位置如右表所示,下列说法错误的是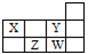
| A.X和Y元素的原子最外层电子数之和等于Z元素的原子最外层电子数的2倍 |
| B.Y元素的非金属性强于W元素的,其最高价氧化物水化物的酸性也强于W的 |
| C.X最简单氢化物溶于水呈碱性,Z最简单氢化物溶于水呈酸性 |
| D.W元素形成的单质可以从Z元素氢化物的水溶液中置换出Z单质 |
B
解析试题分析:根据四种短周期元素在周期表中的相对位置可知,Y是第二周期第ⅦA族元素,所以Y是F,则W是Cl,Z是S,X是N。A、X和Y元素的原子最外层电子数之和等于5+7=12,Z元素的原子最外层电子数是6,因此是2倍关系,A正确;B、同主族自上而下非金属性逐渐增强,最高价氧化物对应水化物的酸性逐渐增强。但F元素是最活泼的非金属,没有含氧酸,B不正确;C、氨气溶于水得到氨水,溶液显碱性。H2S溶于水得到氢硫酸,溶液显酸性,C正确;D、氯元素的非金属性强于硫元素的非金属性,所以氯气能和H2S反应生成氯化氢和单质硫,D正确,答案选B。
考点:考查位置、结构和性质关系的判断

 全能测控一本好卷系列答案
全能测控一本好卷系列答案短周期元素aA2+、bB+、cC3-、dD-都具有相同电子层结构,则下列叙述正确的是( )
| A.原子半径A>B>D>C | B.原子序数D>C>B>A |
| C.离子半径C>D>B>A | D.单质还原性A>B>D>C |
现有四种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5。则下列有关比较中正确的是 ( )
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
根据电子排布的特点,铜元素在周期表属于
| A.s区 | B.p区 | C.d 区 | D.ds区 |
人们对原子结构的认识有一个不断深入的过程,下列先后顺序中符合史实的是( )
①道尔顿提出的原子论 ②卢瑟福的原子结构行星模型
③波尔提出的原子力学模型 ④汤姆生提出的葡萄干面包原子模型
| A.①②④③ | B.①④②③ | C.②①④③ | D.①③②④ |
已知X、Y、Z、W、R是原子序数依次增大的短周期主族元素,X是周期表中原子半径最小的元素,Y元素的最高正价与最低负价的绝对值相等,Z的核电荷数是Y的2倍,W的最外层电子数是其最内层电子数的3倍。下列说法不正确的是
| A.原子半径:Z>W>R |
| B.对应的氢化物的热稳定性:R>W |
| C.W与X、W与Z形成的化合物的化学键类型完全相同 |
| D.Y的最高价氧化物对应的水化物是弱酸 |
如图所示为元素周期表的一部分,X、Y、W、Z均为短周期元素,其中只有X为金属元素。下列说法错误的是
| | W | Z |
| X | Y | |
A.原子半径:Z<W<Y<X
B.元素Y的氧化物能与NaOH溶液反应
C.最简单气态氢化物的热稳定性:Y>X
D.W、Z的氧化物都能与碱反应生成盐和水
下列不能说明氯的非金属性比硫强的事实是 ( )
①HCl比H2S稳定 ②HCl和H2S的水溶液前者的的酸性强
③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
| A.①②④ | B.①②⑥ | C.②⑤ | D.①③⑤ |
下列现象与原子核外电子跃迁无关的是
| A.激光 | B.焰火 | C.核辐射 | D.霓虹灯光 |