下列各组给定原子序数的元素,能形成原子数之比为1∶1稳定化合物的是( )
① 1和6 ② 7和8 ③ 8 和 12 ④ 12和17 ⑤ 20和35
| A.①②④ | B.②③⑤ | C.①②③ | D.③④⑤ |
下列有关物质的性质或结构的说法正确的是( )
| A.L层上的电子数为奇数的原子一定是主族元素的原子 |
| B.周期表中的碱金属元素从上到下,其单质的还原性逐渐增强,熔沸点逐渐升高 |
| C.化学键的形成一定伴随着电子的转移和能量变化 |
| D.元素周期表中,位于金属和非金属分界线附近的元素属于过渡元素 |
短周期元素X、Y、Z、M、R在周期表中的相对位置如图所示。下列说法正确的是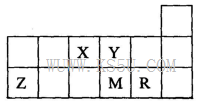
| A.元素X和M的氧化物对应的水化物均为强酸 |
| B.R的单质能与M的氢化物发生置换反应 |
| C.气态氢化物的稳定性:M>Y |
| D.元素Y、Z形成的简单离子半径大小关系为:Z>Y |
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且
M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素)。下列关于这些元素的叙述正确的是( )
| A.X分别和其它四种元素均可形成至少2种化合物 |
| B.M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C.M、X、Z三种元素组成的化合物含有离子键 |
| D.M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙是由X、Y、Z组成的盐。下列说法正确的是
| A.原子半径:W>Y>Z,简单离子半径: Y>Z>W |
| B.YX 3的空间构型是三角锥型,而Y2X4的空间构型类似于乙烯的空间构型 |
| C.测得乙的水溶液呈酸性,则溶液中乙盐阳离子浓度大于酸根离子浓度 |
| D.W的氯化物熔点低,易升华,但水溶液能导电,由此推断它属于弱电解质 |
下列有关元素的性质及其递变规律正确的是( )
| A.IA族与ⅦA族元素间形成的化合物都是离子化合物 |
| B.第三周期元素从左到右,最高正价从+1递增到+7 |
| C.同主族元素的简单阴离子还原性越强,其单质的氧化性越强 |
| D.同周期金属元素的化合价越高,其原子失电子能力越强 |
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,下列说法正确的是
| W | X | |
| | Y | Z |
B.Z元素最高价氧化物对应水化物的酸性一定强于Y
C.X与Y元素的化合价完全相同
D.Z元素单质在化学反应中只表现氧化性
下列说法正确的是
| A.HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B.熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C.NCl3分子中所有的原子均为8电子稳定结构 |
| D.NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |