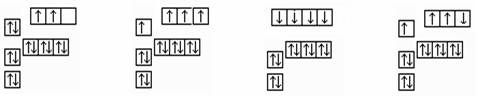
某一个元素质量数是51,中子数是28,其基态原子未成对电子数为
| A.4 | B.1 | C.2 | D.3 |
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙的化学式为YZ3,丙是由X、Y、Z组成的盐。下列说法正确的是
| A.原子半径:W>Y>Z,而离子半径:Z>Y>W |
| B.X的单质分子中存在s-pσ键 |
| C.测得丙的水溶液呈酸性,则溶液中丙盐阳离子浓度大于酸根离子浓度 |
| D.Y的单质分子中有一个p-pσ键和二个p-pπ键 |
R为短周期元素,其原子所具有的电子层数为最外层电子数的一半。下列说法中不正确的是
| A.当它形成含氧酸根离子R2O42—时,也可以形成RO32— |
| B.当它形成含氧酸根离子RO42—时,还可以形成HRO3— |
| C.当它形成含氧酸根离子RO4—时,还可以形成RO3— |
| D.当它形成含氧酸根离子R2O72—时,也可以形成RO42— |
具有下列电子层结构的原子,其相应元素一定属于同一主族的是
| A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 |
| B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 |
| C.最外层电子排布为1s2的原子和最外层电子排布为2s22p6的原子 |
| D.最外层电子排布为1s2的原子和最外层电子排布为2s2的原子 |
几种短周期元素的原子半径及主要化合价见下表:
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.130 | 0.090 | 0.102 | 0.118 | 0.073 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
根据表中信息,判断以下说法正确的是
A.单质与稀硫酸反应的速率快慢:R>Y>X
B.离子半径:T2->X2+
C.元素最高价氧化物对应水化物的碱性:Y>R>X
D.单质与氢气化合的容易程度:Z>T
下列各原子或离子的电子排布式错误的是
| A.K+ 1s22s22p63s23p6 | B.F 1s22s22p5 |
| C.S2- 1s22s22p63s23p4 | D.Ar 1s22s22p63s23p6 |