两种元素原子的核外电子层数之比与最外层电子数之比相等,则在周期表的前10号元素中,满足上述关系的元素共有 ( )
| A.1对 | B.2对 | C.3对 | D.4对 |
氯元素的相对原子质量为35.5,氯只有35Cl和37Cl两种稳定同位素,在氯气中35Cl和37Cl的原子个数比为3∶1,则相对分子质量为70,72,74的氯气分子数之比可能是( )
| A.5∶3∶2 | B.5∶2∶2 | C.5∶2∶1 | D.9∶3∶1 |
下列说法正确的是
| A.第一电离能越小的元素其单质金属活泼性一定越大 |
| B.电负性越小的元素金属性一定越强 |
| C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键 |
| D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低 |
现有四种元素的基态原子的电子排布式如下:① 1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
| A.第一电离能:③>②>① | B.原子半径:③>②>① |
| C.电负性:③>②>① | D.最高正化合价:③>②>① |
下列关于d轨道的说法错误的是
| A.M层才开始出现d轨道 |
| B.d轨道最早出现在第4周期元素 |
| C.电子排布时,3d轨道能量高于4s轨道 |
| D.d轨道有10种空间伸展方向 |
下列表示方法正确的是
A.铜的原子结构示意图: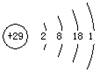 |
| B.S2- 核外电子排布式:[Ne] 2s23p6 |
C.O原子处于基态的轨道表示式: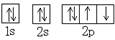 |
D.用电子式表示MgCl2的形成:Mg:+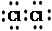 → →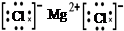 |
在多电子原子中,轨道能量是由以下哪些因素决定
③空间伸展方向④自旋状态
| A.①② | B.①④ | C.②③ | D.③④ |
关于下列图示的说法中正确的是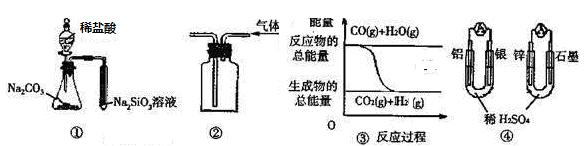
| A.用图 ① 所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
B.用图 ② 所示实验装置排空气法收集CO2气体 | C.图 ③ 表示反应 CO(g)+H2O(g) CO2(g)+H2(g)是放热反应 |
| D.图 ④ 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是 
| A.非金属性:Z<T<X | B.R与Q的电子数相差26 |
| C.气态氢化物稳定性:R <T<Q | D.最高价氧化物的水化物的酸性:T>Q |
X、Y、Z是原子序数依次递增的短周期元素,3种元素的原子核外电子数之和与Ca2+的核外电子数相等,X、Z分别得到一个电子后均形成稀有气体原子的稳定电子层结构。下列说法正确的是
| A.Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 |
| B.原子半径:Z>Y>X |
| C.CaY2与水发生氧化还原反应时,CaY2只作氧化剂 |
| D.CaY2和CaZ22种化合物中,阳离子与阴离子个数比均为1︰2 |