题目内容
关于下列图示的说法中正确的是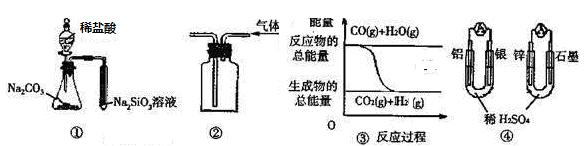
| A.用图 ① 所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
B.用图 ② 所示实验装置排空气法收集CO2气体 | C.图 ③ 表示反应 CO(g)+H2O(g) CO2(g)+H2(g)是放热反应 |
| D.图 ④ 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
C
解析试题分析:A、不能用盐酸,且盐酸易挥发,应用元素最高价氧化物的水化物比较酸性强弱,即此装置不能证明氯、碳、硅三种元素非金属性的强弱,故A错误;B、收集CO2应用向上排空气法,进气管应插入到集气瓶底部,故B错误;C、反应物总能量大于生成物总能量,应为放热反应,故C正确;D、两装置的负极反应分别为Al-3e-=Al3+、Zn-2e-=Zn2+,故通过导线的电子数相同时,消耗负极材料的物质的量不相同,D错误。
考点:考查化学实验基本操作、化学反应与能量、原电池原理等相关知识。

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
短周期元素W、X、Y、Z的原子序数依次增大,W与Y原子的最外层电子数之和为X原子的最外层电子数的2倍,Z原子的最外层电子数等于其最内层电子数,X、Y、Z的简单离子的电子层结构相同,W的单质是空气中体积分数最大的气体。下列说法正确的是
| A.元素Y的气态氢化物比W的稳定 |
| B.元素Y的最高正价与负价绝对值的和等于8 |
| C.化合物XY2与ZY2分子中的化学键类型相同 |
| D.原子半径的大小顺序:r(W)>r(X)>r(Y)>r(Z) |
元素周期表是一座开放的“元素大厦”,“元素大厦”尚未客满。若发现119号元素,请在“元素大厦”中安排好它的“房间”
| A.第七周期0族 | B.第六周期第ⅡA族 |
| C.第八周期第ⅠA族 | D.第七周期第ⅦA族 |
下列各组顺序的排列不正确的是
| A.原子半径:Na>Mg>Al | B.热稳定性:HCl> H2S>PH3 |
| C.还原性:I–<Br–<Cl– | D.熔点:金刚石>食盐>干冰 |
下列各组中两种微粒所含电子数不相等的是
| A.H3O+和OH- | B.CO和N2 | C.HNO2和NO2- | D.CH3+和NH4+ |
下列说法正确的是
| A.第一电离能越小的元素其单质金属活泼性一定越大 |
| B.电负性越小的元素金属性一定越强 |
| C.元素电负性相差小于1.7的元素之间形成的化学键一定为共价键 |
| D.制造光电材料的元素主要从IA族中寻找其主要原因是IA的第一电离能比较低 |
J、Q、M、R、T是原子序数依次增大的短周期主族元素,J、Q、R在周期表中的相对位置如下表。已知J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。下列说法正确的是
| J | | Q |
| | | R |
A. J和氢元素形成的化合物分子中只含极性共价键
B. R、Q两元素形成的氢化物中,R的氢化物沸点更高
C. J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是H2RO4
D. M单质能与氢氧化钠溶液反应,其中水和氢氧化钠都是氧化剂
下列说法正确的是( )
| A.前四周期中,原子最外层为1个电子的元素有5种 |
| B.Fe2+的价电子排布为3d6 |
| C.2p轨道上有1个未成对电子的原子与3p轨道上有1个未成对电子的原子化学性质相似 |
| D.AB3型分子的中心原子A采取sp3杂化 |
