中科院合肥科学岛的专家建成“多功能铅铋堆技术综合实验回路KYLIN—Ⅱ”,该装置是世界最大的多功能液态铅铋综合实验平台,液态金属材料具有高效导热、高沸点、大容量储能的特点,具有广泛的应用前景。下列说法正确的是
| A.液态金属铅中含有离子健 | B.20.7g铅与足量稀盐酸反应生成2.24L氢气 |
| C.可溶性铅盐会引起中毒 | D.液态金属铅是由于其中的氢键作用而形成 |
工业上焙烧明矾[ (SO4)2·12H2O]的化学方程式为:4Al(SO4)2·12H2O+3S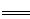 2K2SO4+2Al2O3 +9SO2 +48H2O,下列判断正确的是
2K2SO4+2Al2O3 +9SO2 +48H2O,下列判断正确的是
| A.在焙烧明矾的反应中,还原剂与氧化剂的物质的量之比是3:4 |
| B.最后得到的K2SO4溶液呈中性,所以c(K+)=c(SO42-) |
| C.焙烧产生的SO2可用于制硫酸,焙烧948 t明矾(M=" 474" g/mol),若SO2的利用率为96%,可生产质量分数为98%的硫酸432 t |
D.工业上冶炼Al2O3制得Al,以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是Al+3NiO(OH)+NaOH  NaAlO2+3Ni(OH)2 NaAlO2+3Ni(OH)2 |
下列图示与对应的叙述相符的是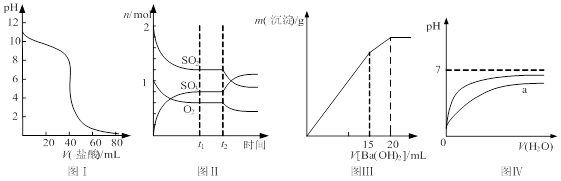
| A.图Ⅰ表示盐酸滴加到0.1 mol/L某碱溶液得到的滴定曲线,用已知浓度盐酸滴定未知浓度该碱时最好选取酚酞作指示剂 |
B.图Ⅱ表示一定条件下进行的反应2SO2+O2 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 2SO3 各成分的物质的量变化,t2时刻改变的条件可能是缩小容器体积 |
| C.图Ⅲ表示某明矾溶液中加入Ba(OH)2溶液,沉淀的质量与加入Ba(OH)2溶液体积的关系,在加入20 mL Ba(OH)2溶液时铝离子恰好沉淀完全 |
| D.图Ⅳ表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是盐酸 |
硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是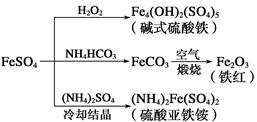
| A.制备碱式硫酸铁利用了过氧化氢的氧化性 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质 |
下列各组稀溶液( )
①NaHSO4和Na2CO3 ②AICl3和NaOH
③NH4HSO4和Ba(OH)2 ④H3PO4和Ca(OH)2
只用试管、滴管及闻气味就能鉴别有几组:
| A.1组 | B.2组 | C.3组 | D.4组 |
下列药品和装置合理且能完成相应实验的是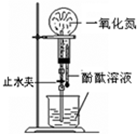
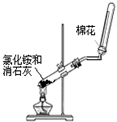
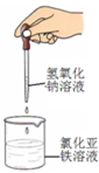
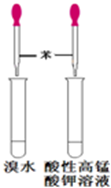
A B C D
| A.喷泉实验 | B.实验室制取并收集氨气 |
| C.制备氢氧化亚铁 | D.验证苯中是否含有碳碳双键 |
下列关于甲、乙、丙、丁四个图像的说法中,正确的是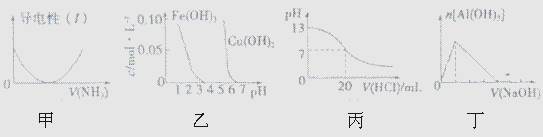
| A.图甲表示向乙酸溶液中通入氨气,此过程中溶液导电性的变化 |
| B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右 |
| C.图丙表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1 mol/L氨水,溶液的pH随加入盐酸体积的变化 |
| D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化 |
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升。根据实验现象判断下列说法错误的是( )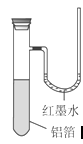
| A.实验中发生的反应都是氧化还原反应 |
| B.铝是一种较活泼的金属 |
| C.铝与氧气反应是放热反应 |
| D.铝片上生成的白毛是氧化铝和氧化汞的混合物 |
A~D是含同一元素的四种物质,它们相互之间有如图所示的转化关系,其中A是单质,D
是氢氧化物,则A可能是( )
①Al ②Mg ③Fe ④Na
| A.①③ | B.①②③ | C.①② | D.②③④ |
