题目内容
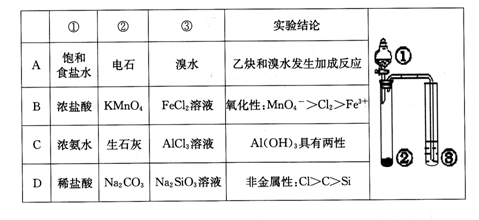
硫酸亚铁是一种重要的化工原料,可以制备多种物质。有关下列制备方法错误的是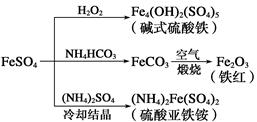
| A.制备碱式硫酸铁利用了过氧化氢的氧化性 |
| B.为防止NH4HCO3分解,生产FeCO3需在较低温度下进行 |
| C.可用KSCN溶液检验(NH4)2Fe(SO4)2是否被氧化 |
| D.制备(NH4)2Fe(SO4)2利用了它的溶解度比FeSO4的溶解度大这一性质 |
D
解析试题分析:A.在FeSO4溶液中Fe是+2价,在碱式硫酸铁中Fe是+3价,向FeSO4溶液中加入过氧化氢制备碱式硫酸铁就是利用了过氧化氢的氧化性。正确。B.NH4HCO3不稳定,受热容易分解,所以为防止NH4HCO3分解,在生产FeCO3需在较低温度下进行。正确。C.若(NH4)2Fe(SO4)2被氧化,则Fe的化合价由+2价变为+3价,检验Fe3+的方法是利用SCN-与Fe3+结合产生血红色的络合物的现象。正确。D.向FeSO4溶液中加入(NH4)2SO4晶体,冷却、结晶就可以产生(NH4)2Fe(SO4)2。是因为(NH4)2Fe(SO4)2在水中的溶解度比FeSO4的溶解度小这一性质。错误。
考点:考查硫酸亚铁的性质及应用的知识。

 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案要使金属晶体熔化必须破坏其中的金属键。金属晶体熔、沸点高低和硬度大小一般取决于金属键的强弱。由此判断下列说法正确的是
| A.金属镁的熔点高于金属铝 |
| B.碱金属单质的熔、沸点从Li到Cs是逐渐升高的 |
| C.金属镁的硬度小于金属钙 |
| D.金属铝的硬度大于金属钠 |
室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是 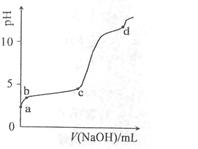
| A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为: Al3++3OH-  Al(OH)3 Al(OH)3 |
| B.a→b段,溶液pH增大,Al3+浓度不变 |
| C.b→c段,加入的OH-主要用于生成Al(OH)3沉淀 |
| D.d点时,Al(OH)3沉淀开始溶解 |
A~D是含同一元素的四种物质,它们相互之间有如图所示的转化关系,其中A是单质,D
是氢氧化物,则A可能是( )
①Al ②Mg ③Fe ④Na
| A.①③ | B.①②③ | C.①② | D.②③④ |
将18 g铜和铁的混合物投入200 mL稀硝酸中,充分反应后得到标准状况下2.24 L NO,剩余9.6 g金属;继续加入200 mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下2.24 L NO。若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法中正确的是( )
| A.原混合物中铜和铁各0.15 mol | B.稀硝酸的物质的量浓度为1 mol·L-1 |
| C.第一次剩余9.6 g金属为铜和铁 | D.再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的浓度为( )
| A.0.5 mol/L | B.3.0 mol/L |
| C.2.0 mol/L | D.1.0 mol/L |
下列有关叙述中正确的是
| A.Mg和Al都可以用电解法冶炼得到 |
| B.Na2O2、Na2O组成元素相同,与CO2反应产物也相同 |
| C.用过量的KSCN溶液除去FeCl2溶液中的少量FeCl3 |
| D.Mg和Fe在一定条件下与水反应都生成H2和对应的碱 |