Cu2S与一定浓度的HNO3反应,生成Cu(NO3)2、CuSO4、NO2、NO和H2O,当NO2和NO的物质的量为2∶1时,则反应中Cu2S与被还原的HNO3的物质的量之比为( )
| A.1∶6 | B.1∶7 | C.1∶8 | D.1∶9 |
在bLFeBr2溶液中通入amolCl2时,使溶液中50%的Br-氧化为Br2,则原FeBr2的物质的量浓度为( )
A.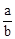 mol·L-1 mol·L-1 | B.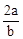 mol·L-1 mol·L-1 | C.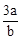 mol·L-1 mol·L-1 | D.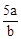 mol·L-1 mol·L-1 |
下列反应都有水参加,其中属于氧化还原反应,而水既不做氧化剂,又不做还原剂的是
| A.2F2+2H2O=4HF+O2 | B.2Na+2H2O=2NaOH+H2↑ |
| C.C12+H2O=HC1O+HC1 | D.C+H2O CO+H2 CO+H2 |
需要加入还原剂才能实现的变化是
| A.MnO2→MnO4— | B.AlO2—→Al(OH)3 | C.AsO43—→AsO33— | D.Cl—→Cl2 |
根据表中信息判断,下列选项不正确的是( )
| 序列 | 参加反应的物质 | 生成物 |
| ① | KMnO4 、H2O2 、H2SO4 | K2SO4 、MnSO4…… |
| ② | Cl2 、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4- …… | Cl2 、Mn2+ …… |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2 与 FeBr2的物质的量之比为1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
NO2通过盛有水的洗气瓶,转移0.03mol电子时,参加反应的NO2气体在标准状况下的体积为
| A.224mL | B.336mL | C.448mL | D.672mL |
下列说法正确的是
| A.HClO中氯元素化合价比HClO4中氯元素化合价低,所以,HClO4的氧化性强 |
| B.已知①Fe + Cu2+ = Fe2+ + Cu;② 2Fe3+ + Cu = 2Fe2+ + Cu2+,则氧化性强弱顺序为: Fe3+ > Cu2+ > Fe2+ |
| C.已知还原性:B- > C-> D-,反应 2C- + D2 = 2D- +C2和反应 2C- + B2 = 2B- +C2都能发生 |
| D.具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
对于Cl2+SO2+2H2O =H2SO4+2HCl反应,下列说法正确的是
①Cl2是氧化剂 ②SO2被氧化 ③Cl2被氧化 ④Cl2发生还原反应
⑤SO2具有还原性 ⑥Cl2具有氧化性
| A.只有①②⑥ | B.只有②③④ | C.只有②④⑤⑥ | D.只有①②④⑤⑥ |
下列叙述正确的是
| A.元素的单质一定是由氧化或还原该元素的化合物制得 |
| B.含有最低价元素的化合物不一定具有很强的还原性 |
| C.阳离子只能得电子被还原,阴离子只能失电子被氧化 |
| D.在化学反应中,得电子越多的氧化剂,其氧化性就越强 |
水热法制备纳米颗粒Y(化合物)的反应为:3Fe2++2S2O32-+O2+a OH-=Y+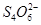 +2H2O下列说法中,不正确的是 ( )
+2H2O下列说法中,不正确的是 ( )
| A.S2O32-是还原剂 | B.Y的化学式为Fe2O3 |
| C.a=4 | D.每有1mol O2参加反应,转移的电于总数为4 mol |