甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含的离子如下表所示:
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH-、NO3—、SO42— |
取等质量的三种化合物配制成相同体积的溶液,其溶质的物质的量浓度:c(甲)>c(乙)>c(丙)。
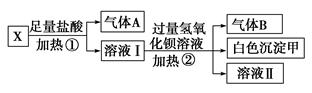
(1)甲是________,向AlCl3溶液中逐滴加入甲溶液,观察到的现象是________,对应的离子方程式为________。
(2)乙是______,设计实验确定乙的物质组成________(若乙已确定,则不填该空)。
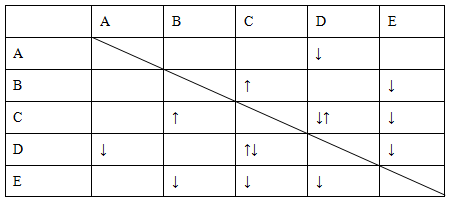
有一种白色粉末,含有下列阴离子和阳离子中的几种。
阴离子:S2-、Cl-、NO、 、
、 、
、 、
、 。
。
阳离子:Na+、Mg2+、Al3+、Ba2+、Fe2+、Fe3+、Cu2+、 。
。
将该白色粉末进行下列实验,观察到的现象如下:
| 实验操作 | 现象 |
| a.取少量粉末,加水、振荡 | 全部溶解、 |
| 溶液无色透明 | |
| b.向所得溶液中慢慢滴入苛性钠溶液,并加热 | 无明显现象 |
| c.取少量粉末,加盐酸 | 无明显现象 |
| d.取少量粉末,加稀H2SO4和稀HNO3的混合液 | 有白色沉淀生成 |
(1)从a实验中,可推断粉末中不可能有 (填离子符号,下同)。
(2)从b实验中,可推断粉末中不可能有 。
(3)从c实验中,可推断粉末中不可能有 。
(4)从d实验中,可推断粉末中不可能有 ,一定含有 。
(5)以上各实验仍无法确定是否存在的离子是 。
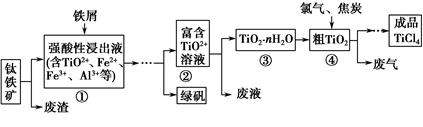
氧化铜矿石含有CuO和Cu2(OH) 2CO3,还含有Fe2O3、FeO和SiO2等。铜、铁是畜禽所必需的微量元素。某饲料厂联合生产硫酸铜和硫酸亚铁工艺流程如下: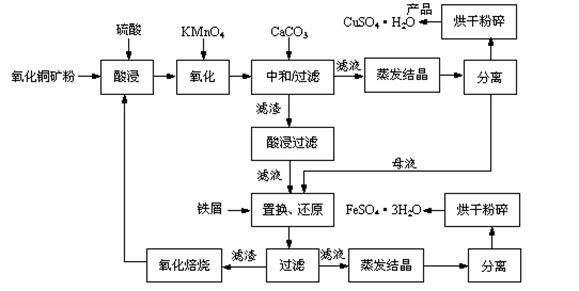
(1)氧化铜矿石粉碎的目的是 。
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的离子方程式 。
(3)“中和/过滤”中加入CaCO3的目的是 。
(4)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 。
(5)加入铁屑的作用是 、 。
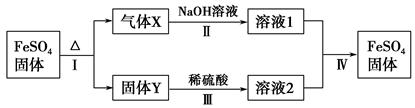
(6)下表和下图为“烘干粉碎”的试验结果。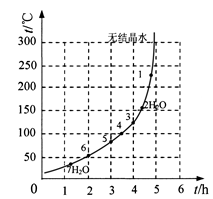
硫酸亚铁干燥曲线图
| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
| 6 | 5 | 160 | 15 | 1 |
表2.硫酸铜晶体(CuSO4·5H2O)干燥试验表
表2中,m为CuSO4·5H2O晶体的质量,x为干燥后所得晶体中结晶水的个数。据此可确定由CuSO4·5H2O和FeSO4·7H2O脱水得流程中所示产品的适宜工艺条件分别为 , (分别指出两条件的温度和时间)。
某无色稀溶液X中,可能含有下表所列离子中的某几种。
| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系图所示。
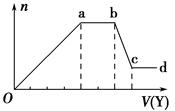
(1)若Y是盐酸,则Oa段转化为沉淀的离子(指来源于X溶液的,下同)是 ,
ab段发生反应的离子是 ,bc段发生反应的离子方程式为 。
(2)若Y是NaOH溶液,则X中一定含有的离子是 ,ab段反应的离子方程式为 。