今有一混合物的水溶液,只可能肯有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成;
(2)第二份加足量NaOH溶液后,收集到气体0.05mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀4.3g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是
| A.K+可能存在 | B.混合溶液中c(CO32-)为1 mol/L |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
下列反应的离子方程式错误的是
| A.等物质的量的Ba (OH)2与NH4HSO4在溶液中反应: Ba2++2OH-+NH4++H++SO42-  BaSO4+NH3?H2O+H2O BaSO4+NH3?H2O+H2O |
B.氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+ Fe3++3H2O Fe3++3H2O |
C.足量的CO2通入饱和碳酸钠溶液中:CO2+CO32-+H2O 2HCO3- 2HCO3- |
D.酸性条件下KIO3溶液和KI溶液反应生成I2:IO3-+5I-+3H2O  3I2+6OH- 3I2+6OH- |
常温时向某溶液中滴入石蕊试液,溶液呈蓝色,其中可能大量共存的离子是
| A.Ag(NH3)2+、K+、Cl-、OH- | B.S2-、Na+、Cl-、ClO- |
| C.Al3+、K+、SO32-、S2- | D.Fe3+、Na+、Cl-、SO42- |
下列化学反应的离子方程式不正确的是
A.Na2S溶液中加入少量FeCl3溶液:2Fe3++S2- 2Fe2++S↓ 2Fe2++S↓ |
| B.向NaOH溶液中滴加碳酸氢钙溶液至OH-恰好完全反应: Ca2++2OH-+2HCO3-  CaCO3↓+2H2O+CO32- CaCO3↓+2H2O+CO32- |
C.向NaClO溶液中通入少量SO2气体:ClO-+SO2+H2O SO42-+Cl-+2H+ SO42-+Cl-+2H+ |
D.Na2CO3溶液中滴入少量邻羟基苯甲酸溶液: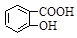 +CO32- +CO32- 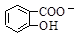 +HCO3- +HCO3- |
根据下表提供的数据可知能大量共存的微粒组是
| 化学式 | 电离常数(25℃) |
| CH3COOH | Ki =1.7×10-5 |
| HClO | Ki =3.0×10-8 |
| H2CO3 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
A.H2CO3、HCO3-、CH3COO-、ClO-
B.HClO、 HCO3-、CH3COO-、ClO-
C.HClO 、HCO3-、ClO-、CO32-
D.HCO3-、CH3COO-、ClO-、CO32-
向含有下列微粒的溶液中分别加入少量NaOH固体、少量浓盐酸或少量酸性高锰酸钾溶液,都能使该微粒浓度下降的是
| A.Fe3+ | B.HS— | C.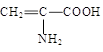 | D.C6H5O— |
某无色溶液中只可能含有①Na+ 、②Ba2+、③Cl一、④I一、⑤SO32一、⑥SO42一 离子中的若干种(忽略水电离出的H+、OH一),依次进行下列实验,且每步所加试剂均过量,观察到现象如下表。下列结论正确的是
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈紫红色 |
| ③ | 向所得水溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
A. 肯定含有的离子是③④⑤ B. 肯定没有的离子是②⑤
C. 可能含有的离子是①⑥ D. 不能确定的离子是③⑥
向10 mL 0.1mol/L NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的
| A.x=10时,溶液中有NH4+、Al3+、SO42—,且c(NH4+)>c(Al3+) |
| B.x=10时,溶液中有NH4+、AlO2—、SO42—,且c(NH4+)>c(SO42—) |
| C.x=30时,溶液中有Ba2+、AlO2—、OH—,且c(OH—)<c(AlO2—) |
| D.x=30时,溶液中有Ba2+、Al3+、OH—,且c(OH—) = c(Ba2+) |
下列化学反应能用离子反应Ca2++ 2HCO3-+ 2OH-→ CaCO3↓+ CO32- + 2H2O表示的是
| A.Ca(OH) 2与少量的NaHCO3 | B.Ca(OH) 2与少量的Ca(HCO3) 2 |
| C.Ca(HCO3) 2与足量的NaOH | D.Ca(OH) 2与足量的Ca(HCO3) 2 |