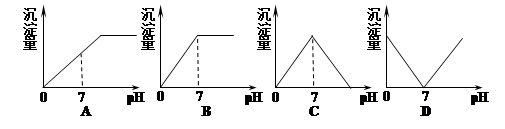向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如下图所示。沉淀的生成与溶解的pH列于下表。以下推断正确的是 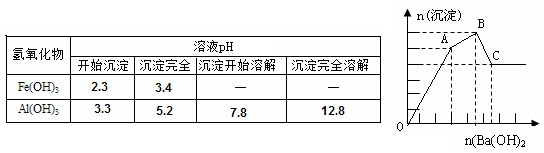
| A.C点的沉淀为:Fe(OH)3 |
| B.OA段可能发生的反应有:3Ba2+ +6OH- +3SO42- +2Fe3+ →3BaSO4↓+2Fe(OH)3↓ |
| C.AB段可能发生的反应是:2SO42- +2Ba2+ +Al3+ +3OH-→2BaSO4↓+Al(OH)3↓ |
| D.据图计算原溶液中c(Cl-)>c(SO42-) |
向Na2CO3溶液中逐滴加入水杨酸(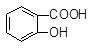 )溶液,可能发生的反应的离子方程式且书写正确的是
)溶液,可能发生的反应的离子方程式且书写正确的是
A.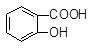 +CO32―→ +CO32―→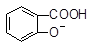 +HCO3― +HCO3― |
B.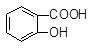 +CO32―→ +CO32―→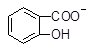 +HCO3― +HCO3― |
C.2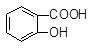 +CO32―→2 +CO32―→2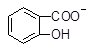 +CO2↑ +CO2↑ |
D.3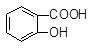 +2CO32―→3 +2CO32―→3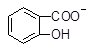 +HCO3―+H2O+CO2↑ +HCO3―+H2O+CO2↑ |
含有下列各组离子的溶液中,滴入过量溴水后仍能大量共存的是
| A.Na+、Fe2+、SO42-、Cl― |
| B.Ag+、Al3+、H+、NO3― |
| C.Na+、K+、SO42-、SO32- |
| D.NH4+、Ca2+、NO3―、Cl- |
下列离子方程式中正确的是
| A.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH- → NH3↑+2H2O |
| B.向FeBr2溶液中通入Cl2,当n(FeBr2)=n(Cl2)时:2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- |
| C.向FeI2溶液中通入Cl2,当n(FeI2):n(Cl2)=1:1时: 2I-+Cl2→I2+2Cl- |
| D.向烧碱溶液中通入CO2,当n(NaOH):n(CO2)=3:2时: OH-+CO2→HCO3- |
下列反应的离子方程式或热化学方程式书写正确的是
| A.除去KNO3溶液中的Fe3+: Fe3++3NH3﹒H2O→Fe(OH)3↓+3NH4+ |
| B.硫酸亚铁溶液中加入过氧化氢溶液:2Fe2++H2O2+2H+→2Fe3++2H2O |
| C.硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO42-→BaSO4↓ |
| D.1L 0.5mol·L-1稀硫酸与1L 1mol·L-1氢氧化钠溶液反应放出57.3kJ的热量:H2SO4(aq)+2NaOH(aq) → Na2SO4(aq)+2H2O(1)+57.3kJ |
下列各组试剂在溶液中反应,当两种试剂的量发生改变时,不能用同一离子方程式表示的是:
| A.苯酚.碳酸钠 | B.硫酸.氢氧化钡 |
| C.氯化铝.氨水 | D.二氧化碳.氢氧化钠 |
实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1 mol/L,下面四个选项中能达到此目的的是
| A.Ca2+、K+、OH?、Cl?、NO3? |
| B.Fe2+、H+、Br?、NO3?、Cl? |
| C.Na+、K+、SO42?、NO3?、Cl? |
| D.Al3+、Na+、Cl?、SO42?、NO3? |
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO—2、CI— |
B.Kw/c( H+) =0.l mol/L的溶液:Na+、K+、Si 、HC 、HC |
C.含有较多S '的溶液:H+、Ca2+、Fe3+、N '的溶液:H+、Ca2+、Fe3+、N |
D.澄清透明溶液中:K+、M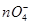 、H3O+、SO42― 、H3O+、SO42― |