题目内容
25℃时,下列各组离子在指定溶液中能大量共存的是
| A.滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO—2、CI— |
B.Kw/c( H+) =0.l mol/L的溶液:Na+、K+、Si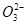 、HC 、HC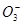 |
C.含有较多S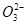 '的溶液:H+、Ca2+、Fe3+、N '的溶液:H+、Ca2+、Fe3+、N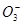 |
D.澄清透明溶液中:K+、M 、H3O+、SO42― 、H3O+、SO42― |
D
解析

练习册系列答案
相关题目
下列实验过程中反应的离子方程式的书写正确的是
| A.水壶中水垢用食醋除去:2H++ CaCO3= Ca2++CO2↑+H2O 2H++Mg(OH)2= Mg2++2H2O |
| B.“84消毒液”(有效成分HClO)和 “洁厕灵”(主要成分盐酸)混用会导致氯气中毒Cl–+ClO–+2H+= Cl2↑+H2O |
| C.SO2通入滴加酚酞的NaOH溶液中,红色变浅:SO2+2NaOH=Na2SO4+ H2O |
| D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+Fe2++14H+=2Cr3++ Fe3++7 H2O |
下列离子或分子组中能大量共存,且满足相应要求的是( )
| 选项 | 离子或分子 | 要求 |
| A | K+、OH-、淀粉、I- | 滴加氯水立即变蓝 |
| B | Fe2+、NO3-、SO42-、H+ | 通C12后加KSCN溶液呈血红色 |
| C | Na+、HCO3-、Ca2+、Cl- | 滴加NaOH溶液立即有沉淀产生 |
| D | K+、NO3-、Cl-、HS- | c(K+)<c(HS-) |
下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使甲基橙呈红色的溶液:Ba2+、A13+、NO3-、C1- |
| B.由水电离出的c(H+)=1×10-11mol·L-1的溶液:Na+、Mg2+、Cl-、NO3- |
| C.0.2 mol·L-1的NaNO3溶液:H+、Fe2+、SO42-、Cl- |
| D.与Fe反应生成H2的溶液:NH4+、K+、SO42-、CO32- |
甲、乙、丙、丁四种易溶于水的物质,分别由Na+、Ba2+、Al3+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知:①0.1 mol/L甲溶液中c(H+)>0.1 mol/L;②将少量乙溶液分别滴入其他三种物质的溶液时,均有白色沉淀生成;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,下列判断正确的是
| A.甲溶液含有SO42- | B.乙溶液含有SO42- |
| C.丙溶液显酸性 | D.丁溶液显酸性 |
下列解释物质用途的反应方程式不正确的是
A.用Fe2(SO4)3净水 Fe3+ + 3H2O Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ |
B.用Na2S处理含Hg2+废水 Hg2+ + S2- HgS↓ HgS↓ |
C.用Na2CO3溶液处理水垢中的CaSO4 Ca2+ + CO32-  CaCO3↓ CaCO3↓ |
D.燃煤时加入石灰石,减少SO2排放 2CaCO3 + 2SO2 + O2 2CaSO4 + 2CO2 2CaSO4 + 2CO2 |
今有一混合物的水溶液,只可能肯有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成;
(2)第二份加足量NaOH溶液后,收集到气体0.05mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀4.3g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是
| A.K+可能存在 | B.混合溶液中c(CO32-)为1 mol/L |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
下列微粒在溶液中能大量共存,通入SO2后仍能大量共存的一组是
| A.Ba2+、Na+、H+、Cl- | B.Na+、K+、SO32-、Cl- |
| C.Al3+、K+、Br-、HCO3- | D.Fe3+、Na+、H2O2、SO42- |
