下列离子在指定溶液中一定能大量共存的是
| A.碱性溶液中:Na+、K+、SO32-、S2- |
| B.无色溶液中:Na+、Fe3+、Cl-、SO42- |
| C.无色溶液中:Na+、K+、HCO3-、AlO2- |
| D.酸性溶液中:Na+、K+、NO3-、ClO- |
下列实验设计及其对应的离子方程式均正确的是
| A.Ca(C1O)2溶液中通入少量SO2气体:Ca2++2C1O—+SO2+H2O=HC1O↓+2HC1O |
| B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| C.向硅酸钠溶液中通入过量的CO2:SiO32-+CO2+H2O=H2SiO3↓+CO32 |
D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO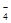 +6H++5H2O2=2Mn2++5O2↑+8H2O +6H++5H2O2=2Mn2++5O2↑+8H2O |
用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2↑的反应个数有
| A.4个 | B.5个 | C.8个 | D.12个 |
能正确表示下列化学反应的离子方程式是( )。
| A.氢氧化钡溶液与硫酸的反应OH-+H+=H2O |
| B.澄清的石灰水与稀盐酸反应Ca(OH)2+2H+=Ca2++2H2O |
| C.铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag |
| D.碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2 |
下列可以大量共存且溶液是无色的离子组是( )。
| A.H+、Na+、NO3-、Cu2+ | B.Ba2+、Mg2+、Cl-、SO42- |
| C.H+、K+、OH-、NO3- | D.NO3-、SO42-、K+、Mg2+ |
一化学兴趣小组在家中进行化学实验,按照①图连接好线路发现灯泡不亮,按照②图连接好线路发现灯泡亮,由此得出的结论正确的是( )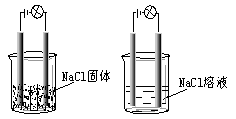
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出了可以自由移动的离子 |
| D.NaCl溶液中水电离出大量的离子 |
下列物质中属于非电解质的是( )。
| A.NaOH | B.O2 | C.Na2CO3 | D.乙醇 |
用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是 ( )
| A.形成较多的白色沉淀 |
| B.形成的沉淀纯度更高 |
| C.排除SO42- 以外的其它阴离子及Ag+的干扰 |
| D.排除Ba2+ 以外的其它阳离子的干扰 |
在某无色酸性溶液中能大量共存的一组离子是
| A.NH4+、SO42-、Al3+、NO3- | B.Na+、K+、HCO3-、NO3- |
| C.Na+、Ca2+、NO3- 、CO32- | D.K+、Cu2+、NH4+、NO3- |
一化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是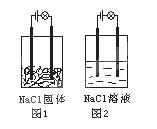
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出可以自由移动的离子 |
| D.NaCl溶液中水电离出大量的离子 |