题目内容
下列离子在指定溶液中一定能大量共存的是
| A.碱性溶液中:Na+、K+、SO32-、S2- |
| B.无色溶液中:Na+、Fe3+、Cl-、SO42- |
| C.无色溶液中:Na+、K+、HCO3-、AlO2- |
| D.酸性溶液中:Na+、K+、NO3-、ClO- |
A
解析试题分析:A.不会发生反应,正确。B.Fe3+呈黄色,错误。C.3(HCO3-)+(Al3+)=3CO2↑+Al(OH)3↓不能共存,错误。D.酸性溶液中:H++ClO-=HClO错误。
考点:考查在指定溶液中离子能否大量共存的等相关知识。

练习册系列答案
相关题目
描述或解释下列现象的离子方程式,不正确的是( )
A.氢氧化钠溶液中滴入紫色石蕊试液,再通入CO2,溶液有蓝变红:CO2+2OH-=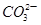 +H2O +H2O |
| B.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O=Fe(OH)3↓+3HClO |
| C.Cl2通入FeBr2溶液中,Cl2与FeBr2物质的量之比4︰5:10Fe2++6Br-+8Cl2=10Fe3++3Br2+16Cl- |
D.碳酸氢铵溶液中加足量澄清石灰水: + +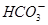 +Ca2++2OH-=CaCO3↓+NH3·H2O+H2O +Ca2++2OH-=CaCO3↓+NH3·H2O+H2O |
下列物质中,不属于电解质的是
| A.蔗糖 | B.NaCl | C.NaOH | D.H2SO4 |
下列有关离子的说法正确的是
| A.H+、NO3-、Fe2+、Na+四种离子在溶液中能够大量共存 |
| B.Cl2通入水中的离子方程式:Cl2+H2O=2H++Cl-+ClO- |
| C.1mol Na2O2中含有2mol阳离子和1mol阴离子 |
| D.向某溶液中加入澄清石灰水变浑浊,再加入盐酸,变澄清且有无色无味气体产生,则原溶液中一定含有碳酸根离子 |
一化学兴趣小组在家中进行化学实验,按照①图连接好线路发现灯泡不亮,按照②图连接好线路发现灯泡亮,由此得出的结论正确的是( )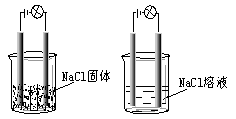
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出了可以自由移动的离子 |
| D.NaCl溶液中水电离出大量的离子 |
下列离子方程式书写正确的是
| A.碳酸钙与盐酸反应 CO32-+2H+=CO2↑+H2O |
| B.硫酸和氯化钡溶液反应 Ba2++SO42-=BaSO4↓ |
| C.氢氧化钠和少量氢硫酸反应 OH-+H2S=S2-+H2O |
| D.铁钉放入硫酸铜溶液中 Fe+3Cu2+=2Fe3++3Cu |
下列表述或化学用语书写正确的是
| A.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性: Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑ |
| C.FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D.金属铝与氧化镁发生铝热反应:2Al+3MgO高温3Mg+Al2O3 |
下列离子方程式书写正确的是
| A.在Fe(OH)3胶体中加入HI溶液:Fe(OH)3 +3H+=Fe3+ +3H2O |
| B.在稀氨水中通入少量SO2:NH3?H2O+SO2=NH4++HSO3- |
| C.向澄清石灰水中加入足量NaHCO3溶液: Ca2+ +OH-+HCO3-=CaCO3↓+ H2O |
| D.在酸性KMnO4溶液中加入H2O2: 2MnO4-+5H2O2 +6H+=2Mn2++5O2↑+ 8H2O |
下列反应的离子方程式书写正确的是( )
A.醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+==Ca2++H2O+CO2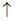 |
B.硫化钠溶于水中:S2-+2H2O H2S+2OH- H2S+2OH- |
| C.过量的NaHSO4溶液与Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
D.用铜作电极电解饱和硫酸铜溶液:Cu+2H2O Cu(OH)2+H2↑ Cu(OH)2+H2↑ |