题目内容
一化学兴趣小组进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是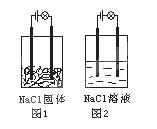
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
| C.NaCl在水溶液中电离出可以自由移动的离子 |
| D.NaCl溶液中水电离出大量的离子 |
C
解析试题分析:电解质是指溶于水或在熔融状态下就能够导电(电解离成阳离子与阴离子)的化合物,电解质溶液导电是因为电解质发生了电离过程,溶液中存在自由移动的离子。A、氯化钠符合电解质的特征,是电解质,故A错误;B、电解质是化合物,不是混合物,因此氯化钠的溶液不是电解质,故B错误;C、NaCl在水溶液中电离出可以自由移动的钠离子与氯离子,是溶液导电的基本条件,故C正确;D、水是弱电解质,在氯化钠的溶液中也不会电离出大量的离子,故D错误,答案选C。
考点:考查电解质判断以及溶液导电性判断

练习册系列答案
相关题目
下列各组离子在指定溶液中能大量共存的是
| A.常温下,呈碱性的溶液:K+、AlO2-、CO32-、Na+ |
| B.含Fe3+的溶液中:K+、NH4+、Cl-、I- |
| C.中性溶液:Fe3+、Al3+、NO3-、SO42- |
| D.无色溶液中:K+、AlO2-、NO3-、HCO3- |
某同学在实验室中进行如下实验:
| 编号 | I | II | III |
| 实验 | 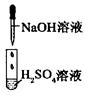 |  | 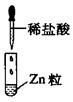 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
A.I中混合前后溶液中各离子种类、个数均不变
B.II中反应前后溶液中Cu2+、Cl-浓度均未变
C.II中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同
D.III中发生的反应属于置换反应,不属于离子反应
下列离子方程式正确的是
| A.氯气通入水中 :Cl2+H2O=2H++Cl-+ClO- |
| B.向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| C.向Fe(NO3)2稀溶液中加入盐酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O |
| D.向NaHCO3溶液中加入少量的Ba(OH)2溶液:Ba2++2HCO3-+2OH-= BaCO3↓+CO32-+2H2O |
下列可以大量共存且溶液是无色的离子组是( )。
| A.H+、Na+、NO3-、Cu2+ | B.Ba2+、Mg2+、Cl-、SO42- |
| C.H+、K+、OH-、NO3- | D.NO3-、SO42-、K+、Mg2+ |
下列离子方程式正确的是
| A.铁与盐酸的反应:Fe + 2H+ = Fe3+ + H2↑ |
| B.碳酸钡溶于醋酸:BaCO3+2H+ = Ba2++H2O+CO2↑ |
| C.铜片插入硝酸银溶液中: Cu +Ag+ = Cu2++ Ag |
| D.硫酸氢钾与氢氧化钠:OH-+H+=H2O |
下列在溶液中各组反应,可用同一离子方程式表示的是( )
| A.氢氧化钠与盐酸;氢氧化钾与碳酸 |
| B.Na2CO3溶液与KHSO4溶液;K2CO3溶液与HCl溶液 |
| C.MgCl2溶液与NaOH溶液;Ba(OH)2溶液与MgSO4溶液 |
| D.氧化钠与稀盐酸混合;氧化铜与稀盐酸 |
下列各组离子在溶液中能大量共存的是
| A.Cu2+、Mg2+、SO42-、NO3- | B.H+、Mg2+、SO42-、ClO- |
| C.Ag+、Na+、NO3-、Cl- | D.NH4+、Ba2+、NO3-、OH- |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.1.0 mol·L-1的CaCl2溶液:Na+、K+、Cl-、CO32- |
| B.1.0 mol·L-1的HNO3溶液:K+、[Ag(NH3)2]+、Cl-、SO42- |
| C.1.0 mol·L-1的KI溶液:Na+、Fe3+、Cl-、SO42- |
| D.澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl- |