向硫酸铝铵溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.NH4+ + SO42—+ Ba2+ +OH— BaSO4↓+ NH3·H2O BaSO4↓+ NH3·H2O |
B.2Al3+ + 3SO42—+3Ba2+ +6OH— 3BaSO4↓+ 2Al(OH)3↓ 3BaSO4↓+ 2Al(OH)3↓ |
C.Al3+ + 2SO42—+ 2Ba2+ + 4OH— 2BaSO4↓+ AlO2—+ 2H2O 2BaSO4↓+ AlO2—+ 2H2O |
D.NH4++Al3+ +2SO42—+2Ba2+ +4OH— 2BaSO4↓+ Al(OH)3↓+ NH3·H2O 2BaSO4↓+ Al(OH)3↓+ NH3·H2O |
解释下列事实的化学用语正确的是
A.将NH3通入滴有酚酞的水中,溶液变红:NH3+ H2O  NH3·H2O NH3·H2O   + OH- + OH- |
B.铜与浓硫酸共热产生气体:Cu+H2SO4(浓) Cu2+ + SO42- + H2↑ Cu2+ + SO42- + H2↑ |
| C.CH3COONa的水溶液呈碱性:CH3COO- + H2O = CH3COOH + OH- |
| D.用NaOH溶液吸收Cl2:Cl2+2OH- = 2Cl- + H2O |
溴是海水中重要的非金属元素,地球上90%的溴元素以Br-的形式存在于海水中,所以人们称溴为“海洋元素”。下列有关说法中正确的是
| A.从海水中提取溴时,不涉及氧化还原反应 |
| B.苯与溴水反应生成溴苯 |
| C.可以用CCl4萃取溴水中的溴 |
| D.向FeBr2溶液中通入Cl2时,一定会发生如下反应: |
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl- |
| B.x=0.6a,2Br-+Cl2=Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2++2Fe3++6Cl- |
下列判断错误的是:( )
| A.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHS04溶液混合,生成白色沉淀:Ba2++SO42?+H++OH? =BaSO4↓+H2O |
| B.常温下,等物质的量浓度的三种溶液①(NH4)2CO3;②NH4Cl;③(NH4)2Fe(SO4)2中c(NH4+):①<②<③ |
| C.加入苯酚显紫色的溶液中:K+、NH4+、Cl-、I- 四种离子不能大量共存 |
D. =1×10-12的溶液: K+、AlO2-、CO32-、Na+四种离子可以大量共存 =1×10-12的溶液: K+、AlO2-、CO32-、Na+四种离子可以大量共存 |
下列方程式中正确的是
| A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I— |
| B.双氧水中滴加2滴FeCl3溶液:2Fe3++H2O2=2Fe2++O2↑+2H+ |
| C.双氧水加入稀硫酸和KI溶液: H2O2+2H++2I—= I2+ O2↑+2 H2O |
| D.在Mg(OH)2悬浊液中滴加氯化铵溶液:Mg(OH)2+2NH4Cl=2NH3·H2O+MgCl2 |
下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl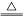 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
C.Na2O2溶于水产生O2:Na2O2+H2O 2Na++2OH-+O2↑ 2Na++2OH-+O2↑ |
D.Ca(HCO3)2溶液与少量NaOH溶液反应: HC+Ca2++OH- CaCO3↓+H2O CaCO3↓+H2O |
下列离子方程式正确的是( )
| A.Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S↓+H2O |
B.磁性氧化铁溶于稀硝酸:3Fe3O4+28H++NO3-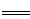 9Fe3++NO↑+14H2O 9Fe3++NO↑+14H2O |
| C.100ml0.1mol/L FeI2溶液与标况下0.224L Cl2: 2Fe2++ Cl2=2Fe3++2Cl- |
| D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -="2" Al(OH)3↓+3BaSO4↓ |
下列说法正确的是(N A表示阿伏加德常数)
| A.1molCu与足量硫反应生成Cu2S,转移的电子数为2 N A |
B.R2+的质量数为A,中子数为N,则ngR该价态的氧化物中含质子数为 N A N A |
| C.氯化铁生成Fe(OH)3胶体的离子方程式:Fe3++3H2O =Fe(OH)3↓+3H+ |
| D.在加入铝片能生成氢气的溶液中一定共存的离子组:Na+、Ba2+、Cl-、NO3- |
