题目内容
下列离子方程式正确的是( )
| A.Na2S2O3溶液中加入稀盐酸:2S2O32-+2H+=SO42-+3S↓+H2O |
B.磁性氧化铁溶于稀硝酸:3Fe3O4+28H++NO3-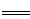 9Fe3++NO↑+14H2O 9Fe3++NO↑+14H2O |
| C.100ml0.1mol/L FeI2溶液与标况下0.224L Cl2: 2Fe2++ Cl2=2Fe3++2Cl- |
| D.向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -="2" Al(OH)3↓+3BaSO4↓ |
B
解析试题分析:A、离子方程式没有配平,O原子不守恒,错误;B、磁性氧化铁为Fe3O4,与H+、NO3?发生氧化还原反应,生成Fe3+、NO和H2O,正确;C、I?还原性大于Fe2+,所以Cl2首先氧化I?,错误;D、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全,KAl(SO4)2与Ba(OH)2的物质的量之比为1:2,所以离子方程式中Al3+与OH?1:4,生成[Al(OH)4]?,错误。
考点:本题考查离子方程式的书写。

练习册系列答案
相关题目
下列说法中用离子方程式表达正确的是
A.用惰性电极电解氯化钠溶液:2Cl-+2H+ H2↑+Cl2↑ H2↑+Cl2↑ |
| B.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3 ↓+CO32- |
| C.Fe(NO3)2溶液中滴加少量稀盐酸:Fe2++NO3-+4H+=Fe3++NO↑+2H2O |
| D.Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-= CaCO3↓+H2O |
下列离子在溶液中能大量共存的一组是( )
| A.Fe3+、H+、ClO-、SO32- |
| B.K+、Al3+、Cl-、CO32- |
| C.Na+、Ca2+、HCO3-、OH- |
| D.Al3+、NH4+、Cl-、SO42- |
向NaHSO3溶液中加入足量Na2O2粉末,充分反应后溶液中离子浓度减少的是(忽略溶液体积变化)
| A.Na+ | B.SO32- | C.OH- | D.SO42- |
在水溶液中能大量共存的一组离子是
| A.Na+、Ba2+、Cl-、NO3- | B.Pb2+、Hg2+、S2-、SO42- |
| C.NH4+、H+、S2O32-、PO43- | D.Ca2+、Al3+、Br-、CO32- |
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是
| A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl- |
| B.x=0.6a,2Br-+Cl2=Br2+2Cl- |
| C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl- |
| D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2++2Fe3++6Cl- |
下列各组离子在给定条件下一定能大量共存的是
A.在c( )=0.1 mol·L-1的溶液中: )=0.1 mol·L-1的溶液中: 、Al3+、Cl-、 、Al3+、Cl-、 |
B.有大量NO存在的强酸性溶液中: 、Ba2+、Fe3+、Cl- 、Ba2+、Fe3+、Cl- |
| C.由水电离出的c(H+)=1×10-12mol·L-1的溶液中:Na+、Al3+、CH3COO-、I- |
| D.能使pH试纸变红的溶液中:ClO-、S2-、Na+、K+ |
下列各组离子在指定的环境中一定能大量共存的是( )。
| A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、SCN- |
| B.含有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I- |
| C.加入铝粉能产生H2的溶液:NH4+、Fe2+、SO42-、NO3- |
| D.含有大量ClO-的溶液:H+、Mg2+、I-、SO42- |
