题目内容
下列方程式中正确的是
| A.FeCl2溶液滴加碘水:2Fe2++I2=2Fe3++2I— |
| B.双氧水中滴加2滴FeCl3溶液:2Fe3++H2O2=2Fe2++O2↑+2H+ |
| C.双氧水加入稀硫酸和KI溶液: H2O2+2H++2I—= I2+ O2↑+2 H2O |
| D.在Mg(OH)2悬浊液中滴加氯化铵溶液:Mg(OH)2+2NH4Cl=2NH3·H2O+MgCl2 |
D
解析试题分析:A、单质碘的氧化性弱于铁离子的,与氯化亚铁不反应,A不正确;B、双氧水在氯化铁的催化作用下发生分解反应生成氧气和水,B不正确;C、双氧水具有强氧化性能把碘化钾氧化生成单质碘,离子方程式为H2O2+2H++2I—=I2+2H2O,C不正确;D、氯化铵与氢氧化镁反应生成一水合氨和氯化镁,D正确,答案选D。
考点:考查离子方程式的正误判断

练习册系列答案
相关题目
某无色溶液中存在大量的H+、NH4+、SO42-,该溶液中还可能存在的离子是
| A.K+ | B.Ba2+ | C.OH- | D.HCO3- |
已知SO32-的还原性大于I-的还原性,某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液组成的判断正确的是
①肯定不含I-;②肯定不含Cu2+;③肯定含有SO32-;④可能含有I-
| A.①③ | B.①②③ | C.③④ | D.②③④ |
在0.1 mol/L的NaHSO3溶液中有如下关系:c(Na+)>c(HSO3-) >c(SO32-) >c(H2SO3),向NaHSO3溶液中慢慢地加入少量的NaOH溶液,发生的主要反应的离子方程式为
A.SO32-+H2O HSO3-十OH— HSO3-十OH— | B.HSO3-十H2O H2SO3十OH- H2SO3十OH- |
C.HSO3-十OH— SO32—十H2O SO32—十H2O | D.H2SO3+OH- HSO3-十H2O HSO3-十H2O |
向硫酸铝铵溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.NH4+ + SO42—+ Ba2+ +OH— BaSO4↓+ NH3·H2O BaSO4↓+ NH3·H2O |
B.2Al3+ + 3SO42—+3Ba2+ +6OH— 3BaSO4↓+ 2Al(OH)3↓ 3BaSO4↓+ 2Al(OH)3↓ |
C.Al3+ + 2SO42—+ 2Ba2+ + 4OH— 2BaSO4↓+ AlO2—+ 2H2O 2BaSO4↓+ AlO2—+ 2H2O |
D.NH4++Al3+ +2SO42—+2Ba2+ +4OH— 2BaSO4↓+ Al(OH)3↓+ NH3·H2O 2BaSO4↓+ Al(OH)3↓+ NH3·H2O |
下列反应的离子方程式书写正确的是
| A.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ═ Al(OH)3↓ |
| B.氢氧化钡溶液与稀 H2SO4:Ba2++OH-+SO42-+H+ ═BaSO4↓+H2O |
| C.向氯化亚铁溶液中通入氯气:2Fe2++Cl2═2Fe3++2Cl- |
| D.过量氯气通入溴化亚铁溶液中2Fe2++2Br-+2Cl2═Fe3++Br2+4Cl- |
下列各组离子因发生氧化还原反应而不能大量共存的是
| A.H+、Fe2+、Cr2O72-、SO42- |
| B.Ca2+、H+、SO42-、HCO3- |
| C.Na+、Cu2+、Cl-、S2- |
| D.Fe3+、K+、SCN-、Cl- |
下列溶液中,一定能大量共存的粒子组是
A.pH=1的溶液中:K+、 、CH3CH2OH、 、CH3CH2OH、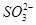 |
B.含有大量Fe3+的溶液中:Al3+、Cu2+、Cl-、 |
C.加入Al能放出H2的溶液中:K+、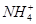 、 、 、Cl- 、Cl- |
D.水电离的c(H+)=10-12 mol/L的溶液中:K+、Ba2+、 、I- 、I- |
下列离子方程式书写正确的是( )
A.过量的SO2通入NaOH溶液中:SO2+2OH-=SO +H2O +H2O |
| B.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
C.NaNO2溶液中加入酸性KMnO4溶液:2MnO +5NO +5NO +6H+=2Mn2++5NO +6H+=2Mn2++5NO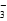 +3H2O +3H2O |
D.NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO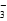 +Ba2++2OH-=BaCO3↓+2H2O+CO +Ba2++2OH-=BaCO3↓+2H2O+CO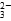 |