题目内容
下列表示对应化学反应的离子方程式正确的是( )
A.MnO2与浓盐酸反应制Cl2:MnO2+4HCl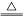 Mn2++2Cl-+Cl2↑+2H2O Mn2++2Cl-+Cl2↑+2H2O |
B.明矾溶于水产生Al(OH)3胶体:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
C.Na2O2溶于水产生O2:Na2O2+H2O 2Na++2OH-+O2↑ 2Na++2OH-+O2↑ |
D.Ca(HCO3)2溶液与少量NaOH溶液反应: HC+Ca2++OH- CaCO3↓+H2O CaCO3↓+H2O |
D
解析试题分析:A、HCl为强电解质,HCl应拆为H+、Cl?,错误;B、明矾溶于水产生Al(OH)3胶体,所以离子方程式中Al(OH)3应注明胶体,错误;C、离子方程式没有配平,O原子不守恒,错误;D、少量的NaOH与Ca(HCO3)2中1个HCO3?反应,正确。
考点:本题考查离子方程式的书写。

练习册系列答案
相关题目
某溶液中含有HCO3-、SO32-、Cl-和Na+,若向其中通入足量的Cl2,溶液中上述四种离子的
浓度基本保持不变的是
| A.HCO3- | B.SO32- | C.Cl- | D.Na+ |
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中,一定能大量共存的是
| A.a点对应的溶液中:Na+、OH-、SO42-、NO3- |
| B.b点对应的溶液中:Al3+、Fe3+,MnO4-、Cl- |
| C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl- |
| D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+ |
下列图示与对应的叙述相符的是
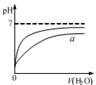
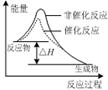

图甲 图乙 图丙 图丁
| A.由图甲表示的反应速率随温度变化的关系可知该反应的ΔH>0 |
| B.图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸 |
| C.图丙表示该反应为放热反应,且催化剂能改变反应的焓变 |
| D.图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
在水溶液中能大量共存的一组离子是( )
| A.HCO3-、H+、NO3-、Na+ |
| B.Na+、Cu2+、OH-、SO42- |
| C.Mg2+、H+、AlO2-、SO42- |
| D.NH4+、K+、Br-、NO3- |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.0. 1mol·L-1NaOH 溶液: K+、Na+、SO42- 、CO32- |
| B.0. 1mol·L-1Na2CO3溶液:K+、Ba2+、NO3- 、Cl- |
| C.0. 1mol·L-1FeCl3溶液:K+、NH4+、I-、SCN- |
| D.c(H+)/c(OH-)= 1×1014的溶液:Ca2+、Na+、ClO-、NO3- |
溴是海水中重要的非金属元素,地球上90%的溴元素以Br-的形式存在于海水中,所以人们称溴为“海洋元素”。下列有关说法中正确的是
| A.从海水中提取溴时,不涉及氧化还原反应 |
| B.苯与溴水反应生成溴苯 |
| C.可以用CCl4萃取溴水中的溴 |
| D.向FeBr2溶液中通入Cl2时,一定会发生如下反应: |
向含有下列各组离子的溶液中通入相应气体后,能大量共存的是
A.通入NO2:Na+、Fe2+、Cl-、 |
B.通入NH3: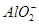 、 、 、Na+、 、Na+、 |
C.通入Cl2:K+、 、I-、Cl- 、I-、Cl- |
D.通入CO2:Na+、K+、 、 、 |
某溶液中存在XO-,且X为短周期元素,则一定能在该溶液中大量共存的离子组是( )。
| A.Na+、H+、SO42-、I- | B.Na+、Ca2+、CO32-、Al3+ |
| C.Na+、K+、Fe2+、H+ | D.K+、SO42-、Cl-、CO32- |