下列离子方程式表达正确的是( )
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HCO3-+H2O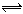 H3O++CO32- H3O++CO32- |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液: |
下列各环境下的离子组合一定能大量共存的是( )
| A.c(HCO3-)=1×10-1mol/L的溶液中Na+、AlO2-、CH3COO-、K+ |
| B.由水电离出的c(H+)=1×10-14mol/L的溶液中CO32-、NH4+、SO42-、K+ |
| C.甲基橙呈红色的溶液中Fe2+、Cl-、NO3-、Na+ |
| D.能使pH试纸呈红色的溶液中Mg2+、Cl-、NO3-、SO42- |
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀生成;
(2)第二份加足量NaOH溶液后,收集到气体0.05mol;
(3)第三份加足量BaCl2溶液后,得干燥沉淀4.3g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,以下推测正确的是( )
| A.K+一定存在 | B.混合溶液中c(CO32-)为1 mol/L |
| C.Cl-一定存在 | D.Ba2+一定不存在,Mg2+可能存在 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使淀粉-KI试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- |
| B.含有0.1mol·L-1Fe2+的溶液:Na+、ClO-、SO42-、Cl- |
| C.c(H+)/c(OH-)=1012的溶液中:Al3+、NH4+、NO3-、K+ |
| D.含有0.1mol·L-1HCO3-的溶液:Na+、Fe3+、NO3-、SO42- |
下列方程式书写正确的是( )
A.碳酸的电离方程式:H2CO3 2H+ + CO32- 2H+ + CO32- |
| B.向氯化钙溶液中通入二氧化硫气体:Ca2+ + SO2 + H2O = CaSO3 ↓+ 2H+ |
| C.往AgI悬浊液中滴加Na2S饱和溶液: 2Ag+ (aq)+ S2-(aq) = Ag2S(s) |
D.明矾水解:Al3+ + 3H2O  Al(OH)3+ 3H+ Al(OH)3+ 3H+ |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.无色溶液中:K+、H+、Fe2+、NO3- |
| B.c(H+)<c(OH-)的溶液中:Na+、K+、SO42-、ClO- |
| C.含0.1mol·L-1 HCO3-的溶液中:Al3+、Ca2+、NO3-、SO42- |
| D.含0.1 mol·L-1 SCN-的溶液中:Fe3+、NH4+、NO3-、Cu2+ |
下列反应的离子方程式正确的是( )
| A.NaHCO3溶液中加入盐酸:CO32-+ 2H+ = CO2↑+ H2O |
B.紫色石蕊试液中滴入氢硫酸变红的原因是:H2S 2H+ + S2- 2H+ + S2- |
| C.将NaHSO4溶液滴入Ba(OH)2溶液中至pH=7:2H+ + SO42-+ 2OH-+ Ba2+ = BaSO4↓+ 2H2O |
D.电解CuSO4溶液:Cu2+ + 2H2O Cu + O2↑+ 4H+ Cu + O2↑+ 4H+ |
下列物质属于强电解质且该状态下能导电的是 ( )
(1)氯化钠溶液; (2)氯化铵固体; (3)铜; (4)石墨;(5)熔融NaOH; (6) 稀硫酸; (7)乙酸;
| A.(1)(2)(5)(6) | B.(5) | C.(2)(5) | D.(1)(3)(4)(5)(6) |
溶液中含有HCO 、SO
、SO 、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
A.HCO | B.SO | C.Cl- | D.Na+ |
下列反应的离子方程式中正确的是
| A.氯气与水反应: Cl2 + H2O= 2H++Cl- +ClO- |
| B.氯气通入氢氧化钠溶液中:2Cl2 + 2OH- =3Cl-+ClO- +H2O |
| C.氯化亚铁溶液中滴加过量新制氯水:2Fe2+ +Cl2 = 2Fe3+ + 2Cl- |
| D.少量碳酸钙固体加入足量稀盐酸中:CO32- +2H+ = CO2↑ + H2O |