题目内容
溶液中含有HCO 、SO
、SO 、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
、Cl-和Na+,若向其中通入足量的Cl2,溶液里上述四种离子的浓度基本保持不变的是 ( )
A.HCO | B.SO | C.Cl- | D.Na+ |
D
解析试题分析:若向含有离子HCO 、SO
、SO 、Cl-和Na+的溶液中通入足量的Cl2,会发生反应Cl2+H2O
、Cl-和Na+的溶液中通入足量的Cl2,会发生反应Cl2+H2O H++Cl-+HClO;HCO3-+H+=CO2↑+H2O;Cl2+H2O+ SO
H++Cl-+HClO;HCO3-+H+=CO2↑+H2O;Cl2+H2O+ SO = 2H++Cl-+SO42-;因此溶液里上述四种离子的浓度基本保持不变的是Na+,选项是D。
= 2H++Cl-+SO42-;因此溶液里上述四种离子的浓度基本保持不变的是Na+,选项是D。
考点:考查溶液中的离子反应和微粒的浓度的关系的知识。

练习册系列答案
相关题目
现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 | | | | | |
(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-=H2O,该离子反应对应的化学方程式为__________________________________________________________。
(3)⑩在水中的电离方程式为_______________________________________________。
(4)少量的④通入⑥的溶液中反应的离子方程式为_______________________________。
(5)②与⑨发生反应的化学方程式为:Al + 4HNO3=Al(NO3)3 + NO↑ + 2H2O,该反应的氧化剂是____________(填化学式),氧化剂与还原剂的物质的量之比是___________,当有5.4g Al发生反应时,转移电子的物质的量为____________。该反应的离子方程式为_____________________________
下列有关叙述中正确的是
| A.难溶于水的电解质一定是弱电解质 |
| B.强电解质在水溶液中的电离过程是不可逆的 |
| C.易溶于水的电解质一定是强电解质 |
| D.强电解质的水溶液导电能力一定比弱电解质水溶液的导电能力强 |
在加入铝粉能放出氢气的溶液中,下列各组离子可能大量共存的是 ( )
A.NH NO NO CO CO Na+ Na+ | B.Na+ Ba2+ Mg2+ HCO |
C.NO K+ AlO K+ AlO OH- OH- | D.NO Mg2+ K+ Cl- Mg2+ K+ Cl- |
离子方程式H+ + OH-= H2O可表示的化学方程式是( )
| A.盐酸与氢氧化铜的反应 | B.硫酸氢钠与氢氧化钠的反应 |
| C.硫酸与氢氧化镁的反应 | D.盐酸与氨水的反应 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A.能使淀粉-KI试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- |
| B.含有0.1mol·L-1Fe2+的溶液:Na+、ClO-、SO42-、Cl- |
| C.c(H+)/c(OH-)=1012的溶液中:Al3+、NH4+、NO3-、K+ |
| D.含有0.1mol·L-1HCO3-的溶液:Na+、Fe3+、NO3-、SO42- |
下列各组离子在溶液中因发生氧化还原反应而不能大量共存的是
| A.NH4+、K+、Cl-、OH- | B.H+、Fe2+、MnO4-、Cl- |
| C.Ba2+、Na+、NO3-、SO42- | D.Na+、H+、CO32-、SO42- |
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol·L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。请根据图像推断,下列说法中不正确的是(已知HCO3-与AlO2-在溶液中不能共存)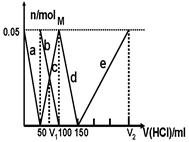
| A.M点时生成的CO2为0 mol |
| B.原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 |
| C.V1:V2=1:4 |
| D.a段表示的离子方程式为:AlO2- +H+ + H2O=Al(OH)3↓ |
在指定的条件下,下列各组离子能大量共存的是( )
| A.使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+ |
| B.强碱性溶液中:K+、Na+、ClO-、S2- |
| C.0.1 mol·L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42- |
| D.由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42- |