用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |
下列各组数值或物理量中,都不随水的“物质的量”的变化而变化的是
| A.水的沸点;水分子的数目 | B.水的密度;水的摩尔质量 |
| C.水的体积;水中所含原子的数目 | D.水的质量;水的相对分子质量 |
右图所示:2个甲分子反应生成1个丙分子和3个乙分子,对此下列判断不正确的是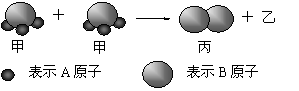
| A.化学反应中分子的种类发生了改变 |
| B.该反应类型是分解反应 |
| C.反应生成的丙物质属于单质 |
| D.根据阿佛加德罗定律可推知,1个乙分子中含有2个A原子 |
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol丙烷分子中,含有的非极性共价键数目为NA |
| B.标准状况下,1.8gH2O分子中所含有的电子数为NA |
| C.25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA |
| D.2.24L氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
下列化学用语使用正确的组合是
A.Mg2+结构示意图: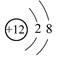 |
B.含18个中子的氯原子的核素符号: Cl Cl |
C.NH4Cl的电子式: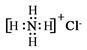 |
D.四氯化碳分子球棍模型:  |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。下列分析或结果错误的是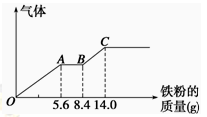
| A.原混合酸中NO3-物质的量为0.1 mol |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)/mol·L-1为
| A.(y-2x)/a mol·L-1 | B.(y-x)/a mol·L-1 |
| C.(2y-2x)/a mol·L-1 | D.(2y-4x)/a mol·L-1 |
某气体的摩尔质量为M g·mol-1,NA表示阿伏加德罗常数的值,在一定的温度和压强下,体积为VL的该气体所含有的分子数为X。则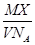 表示的是
表示的是
| A.VL该气体的质量(以g为单位) |
| B.1L该气体的质量(以g为单位) |
| C.1mol该气体的体积(以L为单位) |
| D.1L该气体中所含的分子数 |