题目内容
用NA表示阿伏加德罗常数的值,下列说法正确的是
| A.2.3g金属钠与过量的氧气反应,无论是否加热与否转移电子数均为0.1NA |
| B.1mol Na2CO3晶体中含CO32-离子数小于NA |
| C.惰性电极电解食盐水,若线路中通过NA个电子,则阳极产生气体11.2L |
| D.0.1mol的CaO2中含阴离子数是0.2 NA |
A
解析试题分析:A、钠与氧气的反应为:4Na+O2="===2Na2O" 2Na+O2 Na2O2,无论加热与否,钠元素的化合价 均从0价升高到+1价,所以2.3g金属钠与过量的氧气反应转移电子数均为0.1NA,正确;B、1mol Na2CO3晶体中含CO32-离子数应等于NA;错误;C、缺少条件:标准状况,错误;D、CaO2是由Ca2+和O22-构成的,0.1mol的CaO2中含阴离子数应是0.1 NA,错误。
Na2O2,无论加热与否,钠元素的化合价 均从0价升高到+1价,所以2.3g金属钠与过量的氧气反应转移电子数均为0.1NA,正确;B、1mol Na2CO3晶体中含CO32-离子数应等于NA;错误;C、缺少条件:标准状况,错误;D、CaO2是由Ca2+和O22-构成的,0.1mol的CaO2中含阴离子数应是0.1 NA,错误。
考点:考查阿伏加德罗常数及相关物质的结构和性质

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
二氧化碳、氢气、一氧化碳组成的混合气体在同温、同压下与氮气的密度相同。则该混合气体中二氧化碳、氢气、一氧化碳的体积比为( )
| A.29:8:13 | B.22:1:14 | C.13:8:13 | D.26:12:14 |
用NA代表阿伏加德罗常数的值,下列叙述正确的是( )
| A.7.1 g Cl2与足量NaOH溶液反应,转移的电子数为0.1 NA |
| B.在常温常压下,5.6 L CO中含有的原子数为0.5NA |
| C.4g NaOH固体中含有的离子总数为0.3 NA |
| D.13.5 g Al与足量盐酸反应生成H2的分子数为NA |
将5 mol/L的盐酸10 mL稀释到100 mL,再从中取出5 mL,这5 mL溶液的物质的量浓度为
| A.0.5 mol/L | B.0.25 mol/L | C.5 mol/L | D.1 mol/L |
设NA为阿伏加德罗常数的值,下列叙述中正确的是
| A.1mol丙烷分子中,含有的非极性共价键数目为NA |
| B.标准状况下,1.8gH2O分子中所含有的电子数为NA |
| C.25℃时,pH=13的 Ba(OH)2溶液中含有的OH-数目为0.1 NA |
| D.2.24L氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1NA |
把VL含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁。则原混合溶液中钾离子的浓度为
A.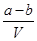 mol·L-1 mol·L-1 | B.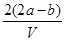 mol·L-1 mol·L-1 |
C.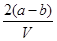 mol·L-1 mol·L-1 | D.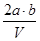 mol·L-1 mol·L-1 |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A.现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3∶2∶1 |
| B.5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C.标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D.n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
下列生活中的现象,不涉及化学变化的是( )
| A.用糯米酿酒 | B.用干冰进行人工降雨 |
| C.用过氧乙酸杀菌消毒 | D.绿色植物的光合作用 |
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此判断下列说法错误的是
| A.该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管. |
| B.取10 mL该硫酸于烧杯中,再加18. 4 mL的水可配得49%的硫酸 |
| C.配制200 mL 4. 6 mol/L的稀硫酸需取该硫酸50 mL‘ |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度小于9. 2 mol/L |