题目内容
某气体的摩尔质量为M g·mol-1,NA表示阿伏加德罗常数的值,在一定的温度和压强下,体积为VL的该气体所含有的分子数为X。则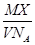 表示的是
表示的是
| A.VL该气体的质量(以g为单位) |
| B.1L该气体的质量(以g为单位) |
| C.1mol该气体的体积(以L为单位) |
| D.1L该气体中所含的分子数 |
B
解析试题分析:根据题给条件,在一定的温度和压强下,体积为VL的该气体所含有的分子数为X,则气体物质的量n= mol,乘以气体摩尔质量得到气体的质量,再除以气体体积得到的是气体的密度。A、以g为单位VL该气体的质量为:
mol,乘以气体摩尔质量得到气体的质量,再除以气体体积得到的是气体的密度。A、以g为单位VL该气体的质量为: mol×Mg?mol-1,故A错误;B、以g为单位1L该气体的质量即气体的密度=
mol×Mg?mol-1,故A错误;B、以g为单位1L该气体的质量即气体的密度= mol×Mg?mol-1/VL=
mol×Mg?mol-1/VL=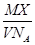 ,故B正确;C、1 mol该气体的体积(以L为单位)=V÷
,故B正确;C、1 mol该气体的体积(以L为单位)=V÷ ,所以C不正确;D、1L该气体所含的分子数=
,所以C不正确;D、1L该气体所含的分子数=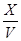 ×NA,故D错误,答案选B。
×NA,故D错误,答案选B。
考点:考查物质的量与微粒数、质量、摩尔质量、气体体积、阿伏伽德罗常数等物理量之间的关系和计算

下列化学用语使用正确的是
| A.石英的化学式:CaCO3 | B.CO2的电子式: |
| C.HClO的结构式:H-O-Cl | D.Mg2+的结构示意图: |
欲配制100 ml 1.0 mol/L Na2SO4溶液,正确的方法是
①将14.2 g Na2SO4 溶于100 ml水中
②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
| A.①② | B.②③ | C.①③ | D.①②③ |
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如下图所示。下列分析或结果错误的是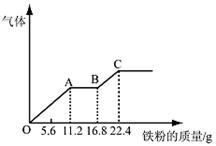
| A.原混合酸中NO3-物质的量浓度为2 mol/L |
| B.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| C.第二份溶液中最终溶质为FeSO4 |
| D.H2SO4浓度为2.5 mol·L-1 |
将51.2 g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8 mol,这些气体恰好能被500 mL 2 mol/L NaOH溶液完全吸收,发生的反应为:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O。则生成的盐溶液中NaNO3的物质的量为
| A.0.2 mol | B.0.4 mol | C.0.6 mol | D.0.8 mol |
向100 mL18 mol·L-1 H2SO4溶液中加入足量的铁片加热。充分反应后,产生的气体在标准状况下的体积为
[提示:2Fe+6H2SO4(浓)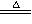 Fe2(SO4)3+3SO2↑+6H2O]
Fe2(SO4)3+3SO2↑+6H2O]
| A.小于20.16 L |
| B.等于20.16 L |
| C.介于20.16 L和40.32 L之间 |
| D.等于40.32 L |
0.8g某物质含有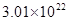 个分子,该物质的相对分子质量约为
个分子,该物质的相对分子质量约为
| A.8 | B.16 | C.64 | D.160 |
某CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),SO42-的物质的量浓度为6mol·L-1,加入足量铁粉充分反应后(忽略溶液体积的变化),c(Fe2+)为
| A.4mol·L-1 | B.6mol·L-1 | C.8mol·L-1 | D.10mol·L-1 |