下列物质的电子式书写正确的是
A.N2: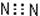 |
B.CO2: |
C.Na2O: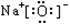 |
D.HCl: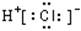 |
下列溶液中的氯离子浓度与50 mL 1 mol?L-1的AlCl3溶液中氯离子浓度相等的是
| A.150 mL 3 mol?L-1的KClO3溶液 |
| B.75 mL 2 mol?L-1的NH4Cl溶液 |
| C.150 mL 2 mol?L-1的CaCl2 溶液 |
| D.350 mL 3 mol?L-1的NaCl溶液 |
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,16gO2和O3的混合气体中含有的原子总数为NA |
| C.标准状况下,11.2LH2O中含有分子的数目为0.5NA |
| D.2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
对相同状况下的12C18O和14N2两种气体,下列说法正确的是( )
| A.若质量相等,则质子数相等 | B.若原子数相等,则中子数相等 |
| C.若分子数相等,则体积相等 | D.若体积相等,则密度相等 |
下列说法正确的是
| A.2.24 L CO2中含有的原子数为0.3×6.02×1023 |
| B.1.8 g NH4+ 含有的质子数为6.02×1023 |
| C.30 g乙酸和甲酸甲酯的混合物中含有的共价键数为4×6.02×1023 |
| D.7.8 g Na2O2中含有的阴离子数为0.2×6.02×1023 |
若两物质恰好完全反应,下列各项中反应前后保持不变的是
①电子总数 ②原子总数 ③分子总数 ④物质的总能量 ⑤物质的总质量
| A.①②⑤ | B.①③⑤ | C.②③④ | D.②④⑤ |
用nA表示阿伏加德罗常数的数值,下列叙述正确的是
| A.常温常压下,200 g 8.5%的H2O2水溶液中含氧原子总数为nA |
| B.标准状况下,22.4LCHCI3中含C -H键数目为nA |
| C.常温下,14g丙烯(CH3CH=CH2)中含碳原子数为nA |
| D.常温下,pH=13的氢氧化钠溶液中,含OH一数目为nA |
下列条件下,两瓶气体所含原子数一定相等的是( )
| A.同质量的C2H4和CO | B.同体积、同密度的C2 H4和C3 H6 |
| C.同温度、同体积的H2和N2 | D.同压强、同体积的N2 O和CO2 |
使用容量瓶配置溶液时,由于操作不当会引起误差,下列情况会使所配溶液浓度偏低的是 ( )
①用天平称量时所用砝码生锈
②用量筒量取所需浓溶液时,仰视刻度
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
| A.②⑤ | B.②③⑥ | C.①⑤⑥ | D.③⑥ |