题目内容
下列条件下,两瓶气体所含原子数一定相等的是( )
| A.同质量的C2H4和CO | B.同体积、同密度的C2 H4和C3 H6 |
| C.同温度、同体积的H2和N2 | D.同压强、同体积的N2 O和CO2 |
B
解析试题分析:A选项, 由N=nNA=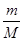 NA知,两种气体的质量相同,摩尔质量相同,所以所含分子数相同,但分子中原子个数不相同,故所含原子数不相等。B选项,同体积同密度的C2H4和C3H6,两种气体的质量相同,由N=nNA=
NA知,两种气体的质量相同,摩尔质量相同,所以所含分子数相同,但分子中原子个数不相同,故所含原子数不相等。B选项,同体积同密度的C2H4和C3H6,两种气体的质量相同,由N=nNA=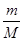 NA知,所含原子数相同,故正确。C选项,压强为确定,故,无法确定。D选项,气体体积受温度压强的影响,因为温度未知,所以同压同体积的N2O和CO2,两种气体的物质的量不一定相等,所含分子数不一定相等,导致所含原子数不一定相等,故错误。
NA知,所含原子数相同,故正确。C选项,压强为确定,故,无法确定。D选项,气体体积受温度压强的影响,因为温度未知,所以同压同体积的N2O和CO2,两种气体的物质的量不一定相等,所含分子数不一定相等,导致所含原子数不一定相等,故错误。
考点:阿伏加德罗定律及推论

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列有关化学用语的表示,正确的是
A.甲烷的电子式: |
B.CCl4分子的比例模型: |
| C.蔗糖与醋酸的最简式相同 |
D.2-甲基丁醇的结构简式: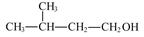 |
已知某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50 mL b mol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是( )
| A.若金属没有剩余,反应中转移的电子数目为2y NA |
| B.若金属全部溶解,则溶液中一定含有Fe3+ |
| C.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80 y(1-a/3) |
| D.若金属全部溶解,且产生336 mL气体(标准状况),则b=0.3 |
500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
| A.(l0b - 5a) mol/L | B.(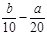 )mol/L )mol/L |
C.(5b一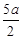 )mol/L )mol/L | D.(2b—a)mol/L |
正确掌握化学用语和化学基本概念是学好化学的基础,下列有关表述中正确的一项是( )
| A.蔗糖与醋酸的最简式相同 |
| B.16O与18O互为同位素,H216O、D216O、H218O、D218O互为同素异形体 |
C.SiH4、CH4、 粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子 粒子的空间构型为正四面体型;CO2、C2H2均为直线型分子 |
D.Ca2+的结构示意图为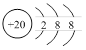 ;NH4Cl的电子式为 ;NH4Cl的电子式为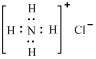 |
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,16gO2和O3的混合气体中含有的原子总数为NA |
| C.标准状况下,11.2LH2O中含有分子的数目为0.5NA |
| D.2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
某乙醇水溶液的质量分数为w%,物质的量浓度为cmol/L,密度为dg/mL,1Kg这种溶液中含有的乙醇是:
| A.46C | B.c/d mol | C.c mol | D.1000dw g |
设nA为阿伏加德罗常数的数值,下列说法错误的是(H:1 O:16) ( )
| A.常温下,1.8g H2O含有0.2nA个H-O 共价键 |
| B.1L 0.3 mol·L-1的FeCl3溶液中Fe3+数目为0.3nA |
| C.标准状况下,22.4 L CCl4中含 nA个CCl4分子 |
| D.标准状况下,22.4 L NO2和CO2的混合气体含有2nA个氧原子 |
下列溶液中的Cl-物质的量与100ml 1 mol·L-1AlCl3溶液中Cl-相等的是
| A.150ml 1 mol·L-1氯化钠溶液 | B.75ml 2 mol·L-1氯化镁溶液 |
| C.50ml 3mol·L-1氯化钾溶液 | D.50ml 1 mol·L-1氯化铁溶液 |