题目内容
用nA表示阿伏加德罗常数的数值,下列叙述正确的是
| A.常温常压下,200 g 8.5%的H2O2水溶液中含氧原子总数为nA |
| B.标准状况下,22.4LCHCI3中含C -H键数目为nA |
| C.常温下,14g丙烯(CH3CH=CH2)中含碳原子数为nA |
| D.常温下,pH=13的氢氧化钠溶液中,含OH一数目为nA |
C
解析试题分析:解答此类题目要注意①理清运算关系:n=N/NA=m/M=V/Vm=cV(aq),②注意相关概念的理解,③注意审题细节。A、忽略了溶剂水中也含有氧原子,200 g 8.5%的H2O2水溶液中含氧原子总数远大于nA,错误;B、标准状况下,CHCI3不是气体,22.4LCHCI3中含C -H键数大于nA,错误;C、常温下,14g丙烯(CH3CH=CH2)中含碳原子数为nA,正确;D、缺少氢氧化钠溶液的体积,无法计算OH一数目,错误。
考点:考查阿伏加德罗常数及以物质的量为中心的计算。

练习册系列答案
相关题目
设NA为阿伏加德罗常数的值,下列有关说法正确的是
| A.1 mol苯分子中含有C=C双键数为3NA |
| B.1 mol甲基(—CH3)所含的电子总数为10 NA |
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为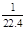 NA NA |
| D.4.2 g乙烯和丙烯的混合气体中所含碳原子数为0.3NA |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温下,23g NO2含有NA个氧原子 |
| B.1 L 0.1 mol·L-1的氨水含有0.1NA个OH- |
| C.标准状况下,22.4 L CCl4含有NA 个CCl4分子 |
| D.1 mol Fe2+与足量的H2O2溶液反应,转移2NA个电子 |
两种金属混合物19.6克,投入到一定量的盐酸中,反应完全后得到11.2L(标准状况)的氢气,此金属混合物不可能是
| A.Mg和Al | B.Al和Fe | C.Mg和Cu | D.Fe和Zn |
设NA为阿佛加德罗常数,下列叙述正确的( )
| A.标准状况下,NA个SO3分子所占的体积约为22.4 L |
| B.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA |
| C.铁粉与一定量的浓硫酸反应,若产生11.2 L SO2和1 g H2,铁粉失去的电子数为2NA |
| D.50 mL 12 mol?L-1浓盐酸与足量二氧化锰反应,转移电子数为0.3 NA |
设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A.12.5mL 16mol·L-1浓硫酸与足量锌反应,转移电子数为0.2NA |
| B.0.1 mol24Mg18O晶体中所含中子总数为2.0 NA |
| C.1L 1 mol·L-1的醋酸溶液中离子总数为2NA |
| D.4.5 g SiO2晶体中含有的硅氧键数目为0.3 NA |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.常温常压下,17g甲基(—14CH3)所含的中子数为9NA |
| B.标准状况下,将2.24L Cl2溶于水,可得到HClO分子的数目是0.1NA |
| C.42.0 g乙烯和丙烯的混合气体中含有的碳原子数为3NA |
| D.5.6g铁与0.1mol氯气在点燃条件下充分反应,转移的电子数为0.3NA |
用NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.标准状况下,22.4LCCl4含有NA个分子 |
| B.常温常压下46gNO2和N2O4混合气体含有3NA个原子 |
| C.0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子 |
| D.0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA |