用NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,2.24 L SO3所含分子数目为0.1NA |
| B.6.0gSiO2中含氧分子的数目为0.1NA |
| C.78g Na2O2固体中含Na+离子的数目为NA |
| D.2.3gNa完全燃烧后失去电子的数目为0.1NA |
与100mL0.1 mol·L—1AlCl3溶液中Cl—的物质的量浓度相等的是
| A.50mL0.1 mol·L—1NaCl溶液 | B.50mL0.15 mol·L—1MgCl2溶液 |
| C.10mL1.0 mol·L—1FeCl3溶液 | D.100mL0.3 mol·L—1KClO3溶液 |
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl— 的物质的量之比为
| A.1∶1∶1 | B.1∶2∶3 | C.3∶2∶1 | D.3∶4∶3 |
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.标准状况下,2.24 L CCl4所含的原子数为0.5 NA |
| B.100 mL 0.1 mol/L的NaCl溶液中,所含微粒总数为0.02 NA |
| C.1.7 g的OH-中含有的电子数为NA |
| D.78 g Na2O2与足量水反应转移电子数为2 NA |
实验室用容量瓶配制480mL的0.1mol·L-1的硫酸铜溶液,以下表述正确的是
| A.称取7.86g硫酸铜 |
| B.称取12.5g胆矾(CuSO4·5H2O) |
| C.容量瓶中原来有少量蒸馏水,使配制溶液的浓度偏低 |
| D.定容时,俯视读数,使配制溶液的浓度偏低 |
NH3和Cl2可快速反应:2NH3+3Cl2 →N2+6HCl 。有100LNH3和Cl2混合气体,充分反应后的混合气体中N2占混合气体的1/7,则N2的物质的量为(标准状况下数据)
| A.0.263 mol | B.0.483 mol | C.0.663 mol | D.0.893 mol |
下列对化学用语的叙述正确的是
| A.碳原子最外层电子云有三种不同的伸展方向 |
B.CCl4的比例模型 |
| C.氮分子的结构式:N≡N: |
D.溴化铵的电子式: 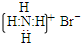 |
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.1mol氯气参加氧化还原反应,转移的电子数一定为2NA |
| B.25℃时,1 L pH=12的Na2CO3溶液中含有Na+的数目为0.02NA |
| C.12 g石墨和C60的混合物中质子总数一定为6NA个 |
| D.常温常压下,22.4L乙烯中C?H键数为4NA |
下列化学用语表述正确的是
A.S2-的结构示意图: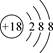 |
B.氮原子的轨道表示式: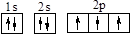 |
C.CO2的比例模型: |
D.氨气分子的结构式: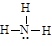 |
碘值是指100 g油脂中所能吸收(加成)碘的克数。测得某植物油碘值为a g,以NA表示阿伏加德罗常数,则b g该植物油中含有的碳碳双键数为
| A.abNA/25400 | B.abNA/12700 | C.abNA/2.54 | D.abNA/1.27 |