设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.常温常压下,32 g甲醇中含有的C—H键的数目为4NA |
| B.标准状况下,11.2 L甲醛中含有的电子数目为8NA |
| C.0.1 mol N2与0.3 mol H2在一定条件下充分反应,生成的氨分子数目为0.2NA |
| D.1 L 0.01 mol·L-1 KAl(SO4)2溶液中,含有的阳离子数目为0.02NA |
下列有关化学用语表示正确的是
A.中子数为20的氯原子: | B.CO2的比例模型: |
C.铝原子的结构示意图: | D.聚丙烯的结构简式: |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1molN2与足量的H2反应,转移的电子数是0.6NA |
| B.常温下, 0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA |
| D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1 N A |
下列有关化学用语表示正确的是
A.四氯化碳分子球棍模型:  |
| B.二氧化硅的分子式:SiO2 |
C.S2-离子结构示意图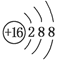 |
D.聚丙烯的结构简式: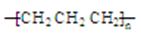 |
下列化学用语正确的是 ( )
A.氯化钠的电子式: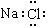 | B.乙烯的结构简式:C2H4 |
C.硅的原子结构示意图: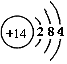 . . | D.硫酸的电离方程式:H2SO4==H22++SO42 |
设NA表示阿伏加德罗常数,下列叙述中正确的是
| A.常温常压下,11.2 LNH3所含的原子数为2NA |
| B.常温常压下,80 g SO3含有的氧原子数为3NA |
| C.标准状况下,22.4 L H2中所含原子数为NA |
| D.一定条件下,56g铁粉与足量的Cl2完全反应转移电子数目为2NA |
体积为1 L的干燥容器中充入HCl气体后,测得容器中气体对氧气的相对密度为1.082。将此气体倒扣在水中,进入容器中液体的体积大约是( )
| A.0.25 L | B.0.5 L | C.0.75 L | D.1 L |
在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气,于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是( )
| A.1∶2 | B.1∶3 | C.1∶4 | D.1∶6 |
有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl- 完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的c(Na+)为( )( mol·L-1)
| A.(y – 2x)/a | B.(y – x)/a | C.(2y – 2x)/a | D.(2y – 4x)/a |
超导材料为具有零电阻及反磁性的物质,以Y2O3、BaCO3和CuO为原料、经研磨烧结可合成一种高温超导物YBa2Cu3Ox,现欲合成0.5 mol此高温超导物,依化学剂量比例,需取Y2O3、BaCO3和CuO的物质的量分别为( )
| A.0.50,0.50,0.50 | B.0.25,1.0,1.5 |
| C.0.50,1.0,1.5 | D.1.0,0.25,0.17 |