题目内容
在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气,于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比是( )
| A.1∶2 | B.1∶3 | C.1∶4 | D.1∶6 |
C
解析试题分析:根据题意知,7.5moL氟气反应剩余4.5mol氟气,反应了3mol氟气,即1.5molXe与3moL氟气反应,根据质量守恒定律知,生成物中氙原子与氟原子物质的量之比为1.5:3×2=1:4,选C。
考点:考查原子守恒法

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列化学用语正确的是
| A.乙烯的结构简式:CH2CH2 | B.氮气分子的结构式:N≡N |
C.F-的结构示意图: | D.NaCl的电子式: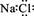 |
明矾[KAl(SO4)2·12H2O]中S元素的化合价是
| A.-2 | B.+2 | C.+4 | D.+6 |
溶于水时,下列物质或微粒对水的电离平衡不产生影响的是
A.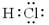 | B.13Al3+ | C.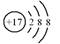 | D.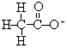 |
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.0.1molN2与足量的H2反应,转移的电子数是0.6NA |
| B.常温下, 0.1 mol·L-1 NH4NO3溶液中含有的氮原子数是0.2NA |
| C.常温常压下,3.2 g O2和3.2 g O3所含氧原子数都是0.2NA |
| D.2.24 L CO和CO2的混合气体中所含的碳原子数为0.1 N A |
下列有关化学用语表示正确的是
A.中子数为20的氯原子: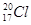 |
B.HClO的电子式: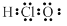 |
C.K2O的电子式: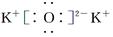 |
D.熔融状态下硫酸氢钾的电离方程式:KHSO4=K++H++SO |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.常温常压下,8gO2含有4NA个电子 |
| B.1L 1mol/L 的NaClO 溶液中含有ClO-的数目为NA |
| C.标准状况下,22.4L盐酸含有NA个HCl分子 |
| D.1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
用NA表示阿伏加德罗常数的值。下列说法正确的是
| A.2.24LCO2中含有的原子数为0.3NA |
| B.1.8g NH4+离子中含有的质子数为NA |
| C.C60和石墨的混合物共1.8g,含碳原子数目为0.15NA |
| D.0.5mol/LNaOH溶液中,含Na+离子数目为0.5NA |
设阿伏加德罗常数(NA)的数值为nA,下列说法正确的是( )
| A.1 mol Cl2与足量Fe反应,转移的电子数为3nA |
| B.1.5 mol NO2与足量H2O反应,转移的电子数为1.5nA |
| C.常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3nA |
| D.0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10nA |