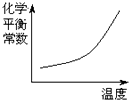
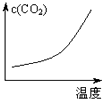
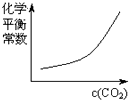
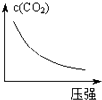
高温下,某反应达到平衡,平衡常数K=
.已知恒容时升高温度,H2的浓度减小.下列说法正确的是( )
| [CO]?[H2O] |
| [CO2]?[H2] |
A、该反应的化学方程式为CO+H2O
| |||
| B、该反应的△H>0 | |||
| C、升高温度,正反应速率增大,逆反应速率减小 | |||
| D、恒温恒容下,增大压强,H2的浓度一定减小 |
在2000K时,反应CO(g)+
O2(g)?CO2(g) 的平衡常数为K1,则相同温度下反应2CO2(g)?2CO(g)+O2(g)的平衡常数K2为( )
| 1 |
| 2 |
A、
| ||
| B、K12 | ||
C、
| ||
D、K1 -
|
反应Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、升高温度该反应的正反应速率增大,逆反应速率减小 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |
下列有关平衡常数说法正确的是( )
| A、温度越高,K值越大 | B、K值越大,反应的转化率越小 | C、K值越大,反应的转化率越大 | D、K值的大小与起始浓度有关 |
对于给定的可逆反应的平衡常数(K)的说法正确的是( )
| A、K只与温度有关,温度不变,K不变 | B、改变条件,反应物的转化率增大,K也一定增大 | C、温度一定时,其正、逆反应的K相等 | D、若正反应△H<0,升高温度,该反应的K增大 |
中学化学涉及多种常数,下列说法正确的是( )
| A、两种物质反应,不管怎样书写化学方程式,平衡常数不变 | ||
B、某温度下,2L密闭容器中加入4mol A和2mol B发生反应:3A(g)+2B(g)?4C(s)+2D( g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=
| ||
| C、温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | ||
| D、难溶电解质AB2饱和溶液中,c(A2+)=x mol?L-1,c(B-)=y mol?L-1,则Ksp值为4xy2 |
在一固定体积的密闭容器中,进行下列反应:CO2(g)+H2(g)?CO(g)+H2O(g)△H=akJ/mol
其化学平衡常数K和温度T的关系如下表所示:
则下列有关叙述正确的是( )
其化学平衡常数K和温度T的关系如下表所示:
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A、a<0 |
| B、可测量客器总压变化来判定化学反应是否达到平衡 |
| C、温度为830℃时,若c(CO2)?c(H2)>c(CO)?c(H2O),此时v正>v逆 |
| D、平衡时,其它条件不变,使用催化剂有利于CO2的转化 |
已知某化学反应的平衡常数表达式为K=
,在不同的温度下该反应的平衡常数数值分别为:
下列有关叙述正确的是( )
| c(CO2)?c(H2) |
| c(CO)?c(H2O) |
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 1.67 | 1.11 | 1.00 | 0.60 | 0.38 |
| A、上述反应的正反应是吸热反应 | ||||
B、该反应的化学方程式是:CO2(g)+H2(g)
| ||||
C、某温度下,如果平衡浓度符合下列关系式:
| ||||
| D、如果在一定体积的密闭容器中加入CO2和H2各1mol,5min后温度升高到830℃,测得CO为0.4 mol时,该反应为平衡状态 |