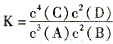题目内容
中学化学涉及多种常数,下列说法正确的是( )
| A、两种物质反应,不管怎样书写化学方程式,平衡常数不变 | ||
B、某温度下,2L密闭容器中加入4mol A和2mol B发生反应:3A(g)+2B(g)?4C(s)+2D( g).平衡时测得n(C)=1.6mol,反应的化学平衡常数表达式为K=
| ||
| C、温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液 | ||
| D、难溶电解质AB2饱和溶液中,c(A2+)=x mol?L-1,c(B-)=y mol?L-1,则Ksp值为4xy2 |
分析:A、平衡常数是用生成物浓度的幂次方乘积除以反应物的幂次方乘积计算,和化学方程式书写有关;
B、固体和液体不写入平衡常数表达式中;
C、沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液;
D、依据沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp;
B、固体和液体不写入平衡常数表达式中;
C、沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液;
D、依据沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp;
解答:解:A、平衡常数是用生成物浓度的幂次方乘积除以反应物的幂次方乘积计算,和化学方程式书写有关,系数变化,平衡常数变化,故A错误;
B、固体和液体不写入平衡常数表达式中,3A(g)+2B(g)?4C(s)+2D( g).平衡常数K=
,故B错误;
C、沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液,温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液,故C正确;
D、沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp,AB2饱和溶液中AB2(s)?A2+(aq)+2B-(aq)Ksp=c(A2+)c2(B-)=xy2,故D错误;
故选C.
B、固体和液体不写入平衡常数表达式中,3A(g)+2B(g)?4C(s)+2D( g).平衡常数K=
| c2(D) |
| c3(A)c2(B) |
C、沉淀溶解平衡状态下离子浓度幂次方乘积等于Ksp达到沉淀溶解平衡,形成饱和溶液,温度一定时,当溶液中(Ag+)?c(Cl-)等于Ksp值时,此溶液为AgCl的饱和溶液,故C正确;
D、沉淀溶解平衡状态下饱和溶液中离子浓度的幂次方乘积计算Ksp,AB2饱和溶液中AB2(s)?A2+(aq)+2B-(aq)Ksp=c(A2+)c2(B-)=xy2,故D错误;
故选C.
点评:本题考查了平衡常数的分析判断主要是表达式书写,沉淀溶解平衡的理解应用,溶度积常数计算式,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
 4C(1)+2D( g)。平衡时测得n(C)=1.6mol ,反应的化学平衡常数表达式为
4C(1)+2D( g)。平衡时测得n(C)=1.6mol ,反应的化学平衡常数表达式为