以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是( )
| A、电能全部转化为化学能 | B、粗铜接电源负极,发生氧化反应 | C、溶液中Cu2+向阳极移动 | D、利用阳极泥可回收Ag、Pt、Au等金属 |
下列关于电解法精炼粗铜的叙述中不正确的是( )
| A、粗铜板与电源的正极相连 | B、电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-=Cu | C、粗铜中所含Ni、Fe、Au、Ag等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 | D、电解铜的纯度可达99.95%~99.98% |
下列说法正确的是( )
| A、电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属 | B、锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后再用酸溶解去除 | C、饱和Ca(OH)2溶液中加入一定量的生石灰,所得溶液的 pH 会增大 | D、反应NH3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行 |
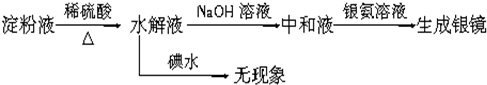
(1)某同学为探究蔗糖的水解反应,进行如下实验,填写实验步骤III的实验现象:
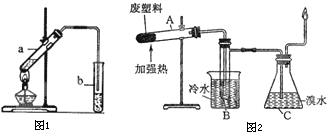
(2)“酒是陈的香”的原因之一是储存过程中生成了有香味的酯.实验室用下图所示装置制取乙酸乙酯.
①试管a中生成乙酸乙酯的化学反应方程式是 .
②试管b中盛放的试剂是 溶液
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是 .
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号) .
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
实验装置如图所示.
①试管A中的最终残余物为 ;
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有 种.
③锥形瓶C中观察到的现象是 ;经溴水充分吸收再干燥后,剩余两种气体的平均相对分子质量为 .
0 60437 60445 60451 60455 60461 60463 60467 60473 60475 60481 60487 60491 60493 60497 60503 60505 60511 60515 60517 60521 60523 60527 60529 60531 60532 60533 60535 60536 60537 60539 60541 60545 60547 60551 60553 60557 60563 60565 60571 60575 60577 60581 60587 60593 60595 60601 60605 60607 60613 60617 60623 60631 203614

| 实验步骤 | 实验现象 |
| I.向编号为①②③的3支试管中,分别加入1mL 20%的蔗糖溶液,向试管②和③中加入0.5mL稀硫酸,并将这3支试管同时水浴加热约5min | 均无明显现象 |
| II.取试管①和②,加入新制氢氧化铜悬浊液,加热至沸腾 | 均无明显现象 |
| III.取试管③,先加入NaOH溶液调溶液pH至碱性,再加入新制氢氧化铜悬浊液,加热至沸腾 | |
| 结论:证明蔗糖在稀硫酸作用下发生了水解反应 | |
①试管a中生成乙酸乙酯的化学反应方程式是
②试管b中盛放的试剂是
③若要把b中制得的乙酸乙酯从混合物中分离出来,应采用的实验操作是
④生成乙酸乙酯的反应是可逆反应,反应物不能完全变成生成物,反应一段时间后,就达到了该反应的限度,也即达到化学平衡状态.下列描述能说明乙醇与乙酸的酯化反应已达到化学平衡状态的有(填序号)
a单位时间里,生成1mol乙酸乙酯,同时生成1mol水
b单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
c单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
d正反应的速率与逆反应的速率相等
e混合物中各物质的浓度不再变化
(3)加热聚丙烯塑料得到的产物如表:
| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 碳 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |
①试管A中的最终残余物为
②试管B收集到的产品中,有能使酸性高锰酸钾溶液褪色的物质,该物质的一氯代物有
③锥形瓶C中观察到的现象是