将元素的原子序数相加可进行有趣的金字塔堆积游戏,如图1 表示丙元素的原子序数等于甲、乙两元素的原子序数之和.利用这种堆积方法,可知图1金字塔中Z元素在元素周期表中的位置为( )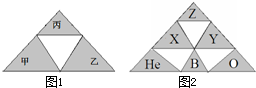

| A、第三周期ⅦA族 | B、第四周期ⅡA族 | C、第三周期ⅠA族 | D、第四周期ⅠA族 |
X、Y均为元素周期表中前18号元素,其简单离子的电子层结构相同,下列说法正确的是( )
| A、X、Y一定不是同周期元素 | B、X2+的氧化性一定大于Y+ | C、由mXa-与nYb+得,m-a=n+b | D、若气态氢化物的稳定性HmX大于HnY,则m>n |
X、Y、Z是周期表中相邻的三种短周期元素,X和Y同周期,Y和Z同主族,三种元素原子的最外层电子数之和为17,核内质子数之和为31,则X、Y、Z是( )
| A、Mg Al Si | B、Li Be Mg | C、N O S | D、P S O |
已知A、B、C、D是原子序数依次增大的短周期主族元素,A、B、C分别在不同周期,A与C同主族,B的一种单质能使带火星的木条复燃,A、C、D三种原子的最外层电子数之和为6.下列说法不正确的是( )
| A、A的原子半径比B的小 | B、B与C形成的化合物只有一种 | C、C在化合物中呈+1价 | D、D单质的晶体可用作半导体材料 |
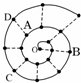 某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“?”代表一种元素,其中起点O代表氢元素.下列说法中正确的是( )
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个弧线上的“?”代表一种元素,其中起点O代表氢元素.下列说法中正确的是( )| A、离O点越远的元素原子半径越大 | B、虚线相连的元素处于同一族 | C、最简单氢化物的热稳定性:A>C>D | D、A、B两种元素组成的化合物中不可能含有共价键 |
已知A、B、C、D、E是短周期原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小;B与E同主族,且E的原子序数是B的两倍;C、D是金属元素,它们的氢氧化物相互之间可以发生反应.下列说法不正确的是( )
| A、单质D可用于冶炼某些难熔金属 | B、工业上常用电解法制得C和D的单质 | C、稳定性:A2B>A2E | D、简单离子的半径:C>D>E>B |
X2YZ6是制造太阳能电池的原材料,X、Y、Z为前20号元素,X+的M层电子数为8,Y元素在地壳中含量居第二位,Z只显-1价,下列说法正确的是( )
| A、气态氢化物的稳定性:Z>Y | B、原子半径:X>Z>Y | C、X的最高价氧化物对应的水化物呈碱性 | D、X2O、YO2两种氧化物含有的化学键类型相同 |
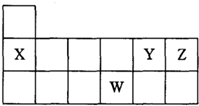 如图是元素周期表的一部分,X、Y、Z、W表示四种短周期元素.下列叙述正确的是( )
如图是元素周期表的一部分,X、Y、Z、W表示四种短周期元素.下列叙述正确的是( )| A、四种元素中,Z的原子半径最小 | B、当Y的化合价为+4时,Y与Z只能形成一种化合物 | C、X的单质极易与氧气反应,通常保存在煤油中 | D、W的氧化物能与强碱反应,但不能与任何酸反应 |
X、Y、Z、M、R、W为六种短周期元素,原子序数依次递增.Y、Z、M是同周期元素,且Z、M最外层电子数之差为1.X+无电子,-ZX是有机物中常见官能团.Y是组成化合物最多的元素,组成为RZX的物质能溶解W2Z3型物质.下列说法不正确的是( )
| A、由X与Y组成的化合物的沸点可能高于由X与Z组成的化合物的沸点 | B、X、Z、R三种元素中的任意两种组合成的(1:1型)物质中均含有共价键 | C、常压条件下,沸点:X2Z2>XM;简单离子半径:Z>M>R>W | D、R3WM6晶体可作为工业电解熔融W2Y3制W单质时的助熔剂 |
六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E同主族,B与F同主族,E与F同周期.已知常温下单质A与E的状态不同,A为气体,E为固体.D的核电荷数是B的最外层电子数的2倍,单质F是一种重要的半导体材料.则下列推断中正确的是( )
| A、A、C两种元素可组成化学式为CA3的化合物 | B、F与D形成的化合物性质很不活泼,不与任何酸反应 | C、原子半径由大到小的顺序是E>F>C>D | D、元素的非金属性由强到弱的顺序是D>C>F>B |