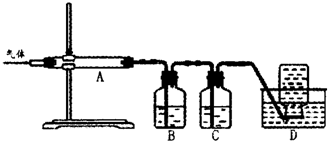
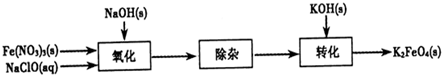
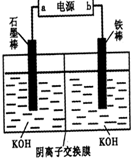
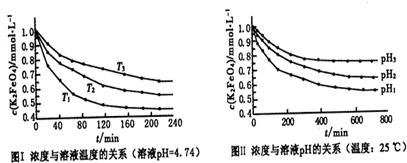
某化学兴趣小组设计以下实验步骤与操作来定性检验茶叶中含有的少量钙、铁、铝三种元素.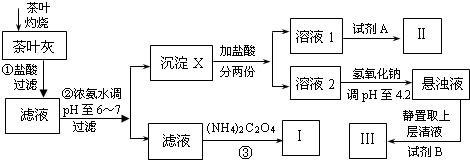
已知Ca2+、Al3+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
(1)步骤①中加入盐酸的作用是 .
(2)步骤②中调节pH至6~7的目的是 .
(3)沉淀X所含主要物质的化学式为 .
(4)写出步骤③中发生反应的离子方程式: .
(5)试剂A为 ;试剂B为铝试剂,加入该试剂后的实验现象是 .

已知Ca2+、Al3+、Fe3+完全形成相应氢氧化物沉淀的pH如下表:
| Ca(OH)2 | Al(OH)3 | Fe(OH)3 | |
| pH | ≥13 | ≥5.2 | ≥4.1 |
(2)步骤②中调节pH至6~7的目的是
(3)沉淀X所含主要物质的化学式为
(4)写出步骤③中发生反应的离子方程式:
(5)试剂A为
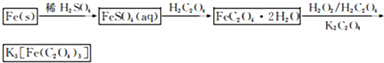
 铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.
铁盐、亚铁盐在工农业生产、生活、污水处理等方面有着极其广泛的应用.(1)用铁屑与稀硫酸反应制备FeSO4
①制备原理用离子方程式表示为
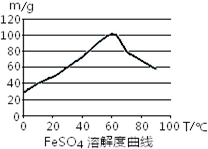
FeSO4生成速率,采取下列措施中正确的是
A.使用浓硫酸与铁屑反应
B.使用磨细的铁粉反应
C.控制温度在50~70℃
D.控制温度在80~100℃
②在上述反应过程中,常会伴随发生反应:4Fe2++O2+4H+?4Fe3++2H2O
若要减少产品FeSO4中Fe3+的含量,采取下列措施中正确的是
A.控制稀硫酸的浓度不能太高
B.用去O2蒸馏水注入浓硫酸配制反应所需的稀硫酸
C.反应中保持n(Fe)/n(H2SO4)>1
D.反应中应经常添加Fe2(SO4)3搅拌
③反应结束后,将溶液进行
(2)工业上用含有少量Cu、Al的废铁屑制备Fe2(SO4)3
其反应及操作流程如下:
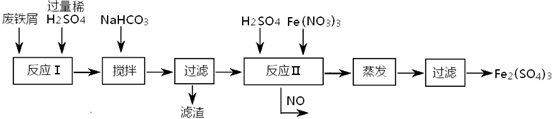
①加入NaHCO3并搅拌,将混合液pH调控至
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 | 4.7 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 | 6.7 |
③生产中,将反应Ⅱ产生的NO配比一种气体X,混合后重新通入反应Ⅱ中,该设计的目的是
(3)用Fe2(SO4)3处理含S2-污水时,有黑色沉淀及淡黄色悬浮物产生,其反应的离子方程式是
实验室中制取下列物质的方案均合理的是( )
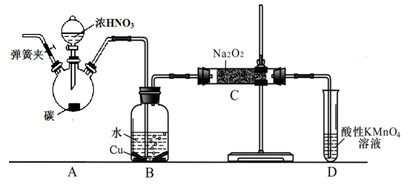
| A、铜和浓硫酸反应,亚硫酸钠和浓硫酸反应均可以制取二氧化硫 | B、铜和浓硝酸反应,碳和浓硝酸反应均可以制取二氧化氮 | C、向氯化铝溶液中加入过量氨水,或加入过量的氢氧化钠溶液均可制取氢氧化铝 | D、向次氯酸钙溶液中通入适量二氧化碳,或通入适量二氧化硫均可制取次氯酸 |
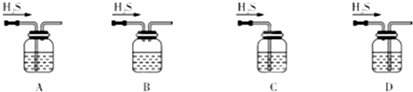
由实验室制备下列物质时,不用加入浓H2SO4的是( )
| A、由苯制取硝基苯 | B、用乙酸和乙醇制备乙酸乙酯 | C、由液溴和苯制取溴苯 | D、由乙醇制乙烯 |
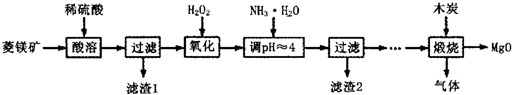
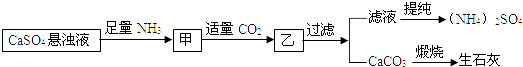
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
下列推断不合理的是( )

下列推断不合理的是( )
| A、直接蒸干滤液得到纯净的(NH4)2SO4 | B、生成1mol(NH4)2SO4至少消耗2molNH3 | C、CO2可被循环使用 | D、往甲中通CO2有利于(NH4)2SO4生成 |
高效净水剂聚合氯化铝铁(PAFC)的组成可表示为[AlFe(OH)nCl6-n]m,该物质广泛应用于日常生活用水和工业废水的净化处理.某工厂欲以工业废料(金属铁、铝及其氧化物)为原料、采用如下流程来制取
PAFC:
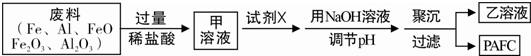
下列判断无法确定的是( )
PAFC:

下列判断无法确定的是( )
| A、PAFC因水解而能净水 | B、往甲溶液中滴入KSCN溶液后呈血红色 | C、试剂X具有氧化性 | D、乙溶液肯定不可能呈强碱性 |