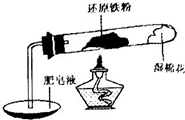
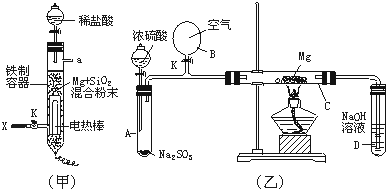
 铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.
铁不能与冷、热水反应,但能与水蒸气反应.中学教材中用下图所示实验装置,完成还原铁粉与水蒸气反应的演示实验.资料显示,在不同温度下,还原铁粉与水蒸气反应的产物是不同的,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4.
(1)实验中使用肥皂液的作用是
(2)甲同学对实验后试管内的黑色固体X含有哪些物质进行了探究.
提出假设:①所得固体是FeO
②所得固体是Fe3O4
③所得固体是
实验探究:
| 实验编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末X放入试管1中,加入盐酸,微热. | 黑色粉末逐渐溶解,有少量气泡产生. |
| ② | 取试管1反应后的溶液少许,滴加几滴KSCN溶液,振荡. | 溶液没有出现血红色. |
| ③ | 取试管1反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡 | 高锰酸钾溶液褪色 |
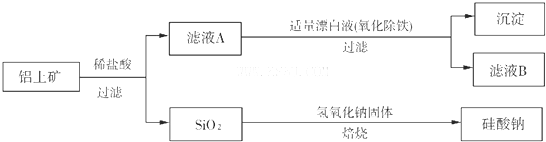
(3)乙同学设计下列实验方案以确定实验后试管内的固体是否存在Fe3O4.
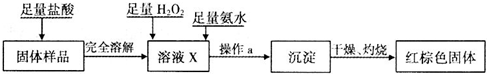
①溶液X中发生氧化还原反应的离子方程式为
②操作a包括过滤和洗涤,检验沉淀是否已经洗涤干净的操作是
③如果取固体样品m1克,反应后得到红棕色固体m2克,则m1与m2之比最少应大于
某课外小组对一些金属单质和化合物的性质进行研究.
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
按反应类型写出实验中发生反应的化学方程式各一个(是离子反应的只写离子方程式)
置换反应 ;
化合反应 .
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡.持续电解,在阴极附近的溶液中还可以观察到的现象是 .
解释此现象的离子方程式是 .
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来.
①用铝与软锰矿冶炼锰的原理是(用化学方程式来表示) .
②MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是 .
0 59883 59891 59897 59901 59907 59909 59913 59919 59921 59927 59933 59937 59939 59943 59949 59951 59957 59961 59963 59967 59969 59973 59975 59977 59978 59979 59981 59982 59983 59985 59987 59991 59993 59997 59999 60003 60009 60011 60017 60021 60023 60027 60033 60039 60041 60047 60051 60053 60059 60063 60069 60077 203614
(1)下表为“铝与氯化铜溶液反应”实验报告的一部分:
| 实验步骤 | 实验现象 |
| 将打磨过的铝片(过量)放入一定浓度的CuCl2溶液中. | 产生气泡,析出疏松的红色固体,溶液逐渐变为无色. |
| 反应结束后分离出溶液备用 | |
| 红色固体用蒸馏水洗涤后,置于潮湿空气中. | 一段时间后固体由红色变为绿色[视其主要成分为Cu2(OH)2CO3] |
置换反应
化合反应
(2)用石墨作电极,电解上述实验分离出的溶液,两极产生气泡.持续电解,在阴极附近的溶液中还可以观察到的现象是
解释此现象的离子方程式是
(3)工业上可用铝与软锰矿(主要成分为MnO2)反应来.
①用铝与软锰矿冶炼锰的原理是(用化学方程式来表示)
②MnO2在H2O2分解反应中作催化剂.若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,该反应的离子方程式是
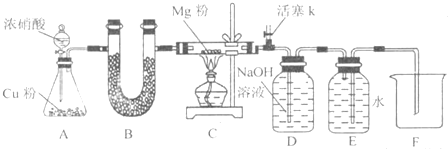
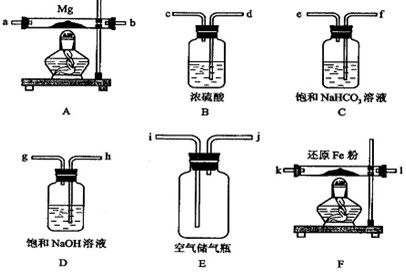

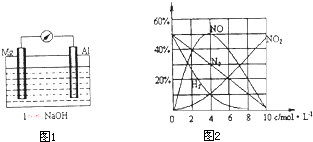
 为了研究铝的某些化学性质及测定某镁铝合金中铝的质量,同学们进行了如下实验:
为了研究铝的某些化学性质及测定某镁铝合金中铝的质量,同学们进行了如下实验: