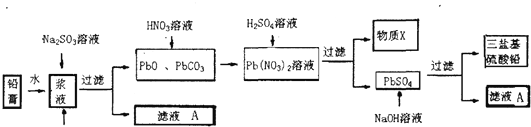
从粗产品硫酸锌固体除去铁、铜、镉等可溶性硫酸盐,从而得到纯净的硫酸锌,实验流程如下: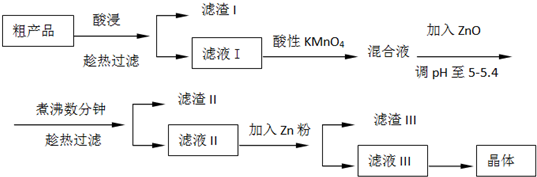
部分阳离子以氢氧化物形式完全沉淀时溶液的pH参见上表,请回答下列问题:
(1)“酸浸”步骤中,为提高锌的浸出率,可采取的措施有 .“酸浸”时适当补充少量水的原因是 .
(2)滤液I加入酸性KMnO4所发生反应的离子方程式为 .加入ZnO的原因是 .
(3)滤渣III的成份主要是 .
(4)从滤液III得到晶体的操作过程为 、冷却结晶、过滤冼涤、小心干燥.

| 沉淀物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Cd(OH)2 | Mn(OH)2 | pH值 | 8.0 | 9.7 | 3.2 | 6.7 | 9.4 | 10.4 |
(1)“酸浸”步骤中,为提高锌的浸出率,可采取的措施有
(2)滤液I加入酸性KMnO4所发生反应的离子方程式为
(3)滤渣III的成份主要是
(4)从滤液III得到晶体的操作过程为
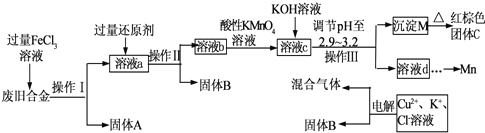
活性氧化锌常用作橡胶制品的硫化活性剂.工业上用粗氧化锌(含少量CuO、FeO、MnO、Fe2O3等)生产活性氧化锌,生产工艺流程如下:
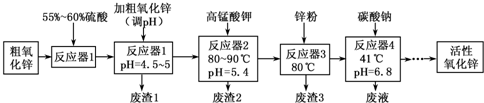
根据上表提供的信息,回答下列问题:
(1)“废渣1”的主要成分是 .
(2)完成“反应器2”中反应之一的离子方程式: MnO 4-+ Mn2++ = MnO2↓+ H+
(3)蘸取“反应器2”中的溶液点在 试纸上,如果观察到试纸变蓝,说明KMnO4过量.
(4)“废渣2”分离出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)=2MnO(s)+CO2(g)△H=-174.6kJ?mol-1
C(s)+CO2(g)=2CO(g)△H=+283.0kJ?mol-1
试写出MnO2(s)与CO(g)反应制取MnO(s)的热化学方程式: .
(5)“反应器3”中加入锌粉的作用是 .
(6)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有 .
(7)从“反应器4”中经过滤等操作得到碱式碳酸锌.取碱式碳酸锌3.41g,在400~450℃下加热至恒重,得到ZnO 2.43g和标准状况下CO2 0.224L,碱式碳酸锌的化学式为 .

| Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
| 开始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
| 沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
(1)“废渣1”的主要成分是
(2)完成“反应器2”中反应之一的离子方程式:
(3)蘸取“反应器2”中的溶液点在
(4)“废渣2”分离出的MnO2可用于制取MnO,已知:
2MnO2(s)+C(s)=2MnO(s)+CO2(g)△H=-174.6kJ?mol-1
C(s)+CO2(g)=2CO(g)△H=+283.0kJ?mol-1
试写出MnO2(s)与CO(g)反应制取MnO(s)的热化学方程式:
(5)“反应器3”中加入锌粉的作用是
(6)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有
(7)从“反应器4”中经过滤等操作得到碱式碳酸锌.取碱式碳酸锌3.41g,在400~450℃下加热至恒重,得到ZnO 2.43g和标准状况下CO2 0.224L,碱式碳酸锌的化学式为
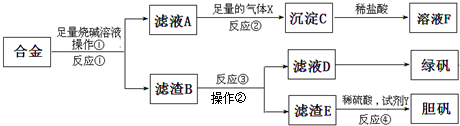
为了确定一批合金废料的成分并加以回收利用,某同学拟定了如图实验方案:
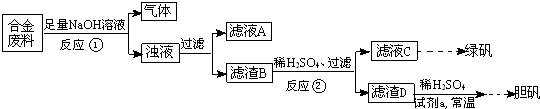
请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe 和 (填化学式).
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为 ;滤渣D、稀硫酸和试剂a总反应的化学方程式为 .
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na4SiO4(H4SiO4白色胶状沉淀)的方法是:取少量滤液A于试管中,滴加 .
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的
NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
①实验①最先溶解的金属是 ;
②实验④中金属全部溶解后,再发生的反应是Fe2+和HNO3,则滤渣B中Fe的质量分数为 %(精确到0.1%).

请回答下列问题:
(1)从上述信息可确定该合金中一定含有Fe 和
(2)“试剂a”是一种不引入杂质的绿色氧化剂,该氧化剂的化学式为
(3)若反应①产生的气体是H2,则验证滤液A只含NaAlO2、不含Na4SiO4(H4SiO4白色胶状沉淀)的方法是:取少量滤液A于试管中,滴加
(4)取质量均为13.2g的滤渣B四份,分别加入相同浓度,不同体积的稀HNO3充分反应,标准状况下所生成的
NO(设还原产物只有一种)体积与剩余固体金属的质量如下表:
| 实验编号 | ① | ② | ③ | ④ |
| 稀HNO3体积(mL) | 100 | 200 | 300 | 400 |
| 剩余金属质量(g) | 9.0 | 4.8 | 0 | 0 |
| NO体积(L,标况) | 1.12 | 2.24 | 3.36 | 4.48 |
②实验④中金属全部溶解后,再发生的反应是Fe2+和HNO3,则滤渣B中Fe的质量分数为
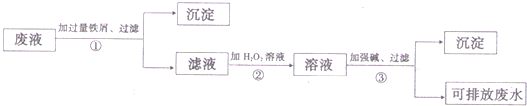
某化学研究性小组同学提出回收含铜废电缆中铜单质的两种方案,并向老师咨询,老师就以下几个方面的问题与同学们展开讨论.
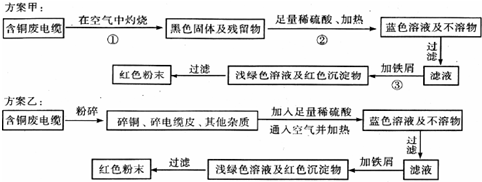
(1)符合绿色理念的方案是 (填“方案甲”或“方案乙”),理由是 .
(2)老师建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是 .
(3)老师建议同学们用化学方法检验红色粉末中是否含有过量的铁屑.请完成表格相关内容:
(4)为了提高原料的利用率,老师建议把最后一步所得浅绿色滤液通过蒸发、冷却结晶、过滤、洗涤、自然干燥得到一种带结晶水的硫酸亚铁晶体.研究小组按老师的建议完成上面操作步骤,获得晶体后对其进行检测.
①取ag晶体进行脱水实验,获得无水固体(a-1.26)g;
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加(10.00mL)溶液时,恰好完全沉淀.研究小组通过计算测知该晶体的化学式是 .

(1)符合绿色理念的方案是
(2)老师建议,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑,目的是
(3)老师建议同学们用化学方法检验红色粉末中是否含有过量的铁屑.请完成表格相关内容:
| 序号 | 实验操作 | 实验现象 | 离子方程式 |
| ① | 取适量的样品于试管内 | ||
| ② | 用滴管滴入足量硫酸溶液,并充分振荡试管 | ||
| ③ | 溶液先变黄色,滴入KSCN溶液后,溶液变红色 |
①取ag晶体进行脱水实验,获得无水固体(a-1.26)g;
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加(10.00mL)溶液时,恰好完全沉淀.研究小组通过计算测知该晶体的化学式是
工业上可以从电解铜的阳极泥中提取很多重要物质,其工艺流程如下:
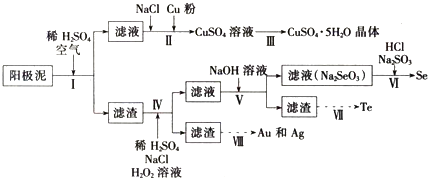
已知:①阳极泥的主要化学成分,如表所示
②温度和硫酸浓度对阳极泥中各组分浸出率的影响,如表所示
(1)步骤I的主要目的为浸出铜,此过程中发生的主要反应的化学方程式为 ,分析表2数据,可知步骤I最适合的条件为 .
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为 .
(3)步骤Ⅲ的操作方法为 .
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为 ;此过程中H2O2溶液的添加量要远远高于理沧值,原因为 .
(5)步骤Ⅵ中所发生反应的化学方程式为 .
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为 .
(7)步骤Ⅷ中得到的Au和Ag混合物可以用 进行分离(填选项字母).
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水.
0 59728 59736 59742 59746 59752 59754 59758 59764 59766 59772 59778 59782 59784 59788 59794 59796 59802 59806 59808 59812 59814 59818 59820 59822 59823 59824 59826 59827 59828 59830 59832 59836 59838 59842 59844 59848 59854 59856 59862 59866 59868 59872 59878 59884 59886 59892 59896 59898 59904 59908 59914 59922 203614

已知:①阳极泥的主要化学成分,如表所示
| 主要成分 | Cu | Ag | Au | Se | Te |
| 百分含量/% | 23.4 | 12.1 | 0.9 | 6.7 | 3.1 |
| 固定浸出温度 | 固定H2SO4浓度 | |||||||||||
| H2SO4浓度/mol?L-1 | 浸出率/% | 浸出温度/℃ | 浸出率/% | |||||||||
| Cu | Ag | Au | Se | Te | Cu | Ag | Au | Se | Te | |||
| 4 | 95.1 | 4.67 | <0.2 | 0.83 | 8.93 | 30 | 87.1 | 4.58 | <0.2 | 0.08 | 6.83 | |
| 3 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | 40 | 94.5 | 4.65 | <0.2 | 0.28 | 6.90 | |
| 2 | 78.1 | 2.65 | <0.2 | 0.05 | 2.85 | 50 | 96.1 | 5.90 | <0.2 | 0.64 | 8.73 | |
(2)步骤Ⅱ中,加入Cu粉的目的是除去滤液中含碲的离子,加入NaCl的目的为
(3)步骤Ⅲ的操作方法为
(4)步骤Ⅳ中,反应温度为75℃.加入H2O2溶液的作用为
(5)步骤Ⅵ中所发生反应的化学方程式为
(6)步骤Ⅶ中,Te的获得可以通过碱性环境下电解Na2TeO3溶液实现,其阴极的电极反应式为
(7)步骤Ⅷ中得到的Au和Ag混合物可以用
A.稀硝酸 B.浓盐酸 C.浓氢氡化钠溶液 D.王水.