(1)与OH-电子数和质子数均相同的单核微粒的离子结构示意图为 ;
(2)要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是 (填选项);
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
A.①③B.③②C.③①D.①②③
(3)25℃时,2.3g酒精在血液中被氧气完全氧化放出66.8kJ热量,该反应的热化学方程式为 ;
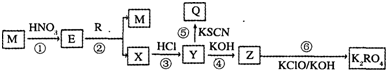
(4)汽车安全气囊中含MYn和红棕色金属氧化物.M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生如图的转化.
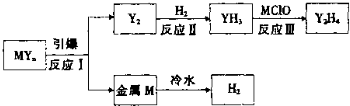
①在2L密闭容器中,起始投入2mol Y2和3.5mol H2发生反应Ⅱ,测得平衡时的数据如表.若该反应△H<0,则T1 T2(填“>”、“<”或“=”);在温度T2下,若经过10min反应达到平衡,则平均速率v(YH3)= ,平衡常数为 ;(保留两位有效数字)
②反应Ⅲ的化学方程式为 ;
③红棕色金属氧化物是为消除反应Ⅰ生成的金属M,该反应的化学方程式为 .
0 22419 22427 22433 22437 22443 22445 22449 22455 22457 22463 22469 22473 22475 22479 22485 22487 22493 22497 22499 22503 22505 22509 22511 22513 22514 22515 22517 22518 22519 22521 22523 22527 22529 22533 22535 22539 22545 22547 22553 22557 22559 22563 22569 22575 22577 22583 22587 22589 22595 22599 22605 22613 203614
(2)要证明某溶液不含Fe3+但可能含有Fe2+,最佳的实验操作顺序是
①加入少量氯水②加入足量KMnO4溶液③加入少量NH4SCN溶液
A.①③B.③②C.③①D.①②③
(3)25℃时,2.3g酒精在血液中被氧气完全氧化放出66.8kJ热量,该反应的热化学方程式为
(4)汽车安全气囊中含MYn和红棕色金属氧化物.M、Y为短周期元素,其最外层电子数之和等于氧原子的最外层电子数,且可发生如图的转化.

①在2L密闭容器中,起始投入2mol Y2和3.5mol H2发生反应Ⅱ,测得平衡时的数据如表.若该反应△H<0,则T1
| 温度 | 平衡时YH3的物质的量(mol) |
| T1 | 1.2 |
| T2 | 1.0 |
③红棕色金属氧化物是为消除反应Ⅰ生成的金属M,该反应的化学方程式为
 单质X、Y与化合物甲、乙有如图1所示的转化关系(必要的反应条件未标出),回答下列问题:
单质X、Y与化合物甲、乙有如图1所示的转化关系(必要的反应条件未标出),回答下列问题: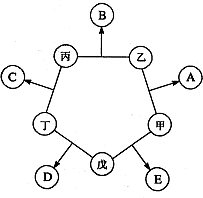 甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.
甲、乙、丙、丁、戊五种单质在一定条件下反应生成A、B、C、D、E五种化合物,其转化关系如图所示:又知:①甲、乙、丙、丁均为前三周期元素的单质,常温下均为气态,丙、丁是空气的主要成分,戊是日常生活中一种常见的金属.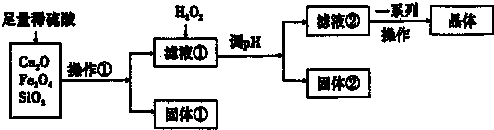
 ( I)某无色稀溶液X中,可能含有下表所列离子中的某几种.
( I)某无色稀溶液X中,可能含有下表所列离子中的某几种. ,其含苯环的同分异构体共有
,其含苯环的同分异构体共有