硫代硫酸钠(Na2S2O3)可看成是一个S原子取代了Na2SO4中的一个O原子而形成.研究小组运用类比学习的思想,通过实验探究Na2S2O3的化学性质.
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是 .
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
(3)小组同学为确证经操作三后Na2S2O3被氧化,提出如下实验方案 .
(1)他们提出如下猜想:猜想①:与BaCl2溶液反应有沉淀生成;猜想②:溶液呈中性,且不与酸反应;猜想③:无还原性,不能被氧化剂氧化.
他们提出上述猜想的依据是
(2)对上述猜想②、③,他们设计实验方案,并进行实验.请在答题卡上按下表格式完成相关的实验操作步骤、预期现象.请限选实验仪器与试剂:试管、玻璃棒、滴管、pH试纸:3mol?L-1H2SO4、新制氯水、1mol?L-1 BaCl2 溶液、Na2S2O3溶液、蒸馏水.
| 实验操作 | 实验现象或 预期实验现象 |
现象解释 (用离子方程式表示) |
结论 | |
| 猜想② | 操作一: |
溶液pH=8 | / | Na2S2O3溶液呈中性,能与酸反应,具有还原性,与Na2SO4的化学性质不相似. |
| 操作二: |
S2O32-+2H+=S↓+SO2↑+H2O | |||
| 猜想③ | 操作三: |
某化学活动小组探究SO2、CO2对品红溶液是否都有漂白作用.
【实验原理】
利用碳酸盐和亚硫酸盐分别与酸反应可以生成CO2和SO2,然后让两种气体直接与品红溶液作用.
【实验装置】
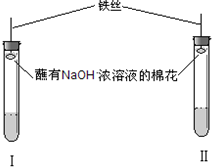
【实验操作和现象】
①请你判断两种气体对品红的漂白性,并将你的结论填写在上表中.
②该实验装置中胶塞上都附着蘸有浓NaOH溶液的棉花,其作用是: .
【问题探究】
他们推测品红可能是一种酸碱指示剂
①你认为他们推测的依据是 .
②请你帮助他们设计实验验证上述推测.实验方案: .
【问题延伸】
某同学将SO2通入酸性高锰酸钾溶液,溶液紫色褪去.他认为该现象表现出SO2的漂白性,你认为正确吗?若不正确,请回答原因;若正确,此空不答 .
0 22279 22287 22293 22297 22303 22305 22309 22315 22317 22323 22329 22333 22335 22339 22345 22347 22353 22357 22359 22363 22365 22369 22371 22373 22374 22375 22377 22378 22379 22381 22383 22387 22389 22393 22395 22399 22405 22407 22413 22417 22419 22423 22429 22435 22437 22443 22447 22449 22455 22459 22465 22473 203614
【实验原理】
利用碳酸盐和亚硫酸盐分别与酸反应可以生成CO2和SO2,然后让两种气体直接与品红溶液作用.
【实验装置】

【实验操作和现象】
| 实验操作 | 实验现象 | 探究结论 |
| A.取少量品红溶液加入试管Ⅰ中,加入适量碳酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红色 | CO2 |
| B.取少量品红溶液加入试管Ⅱ中,加入适量亚硫酸钠溶液,充分混合后再加入一定量的稀硫酸,并立即塞上塞子 | 溶液的红色逐渐褪去,加稀硫酸后溶液逐渐变红,随着反应的进行,颜色又逐渐消失 | SO2 |
②该实验装置中胶塞上都附着蘸有浓NaOH溶液的棉花,其作用是:
【问题探究】
他们推测品红可能是一种酸碱指示剂
①你认为他们推测的依据是
②请你帮助他们设计实验验证上述推测.实验方案:
【问题延伸】
某同学将SO2通入酸性高锰酸钾溶液,溶液紫色褪去.他认为该现象表现出SO2的漂白性,你认为正确吗?若不正确,请回答原因;若正确,此空不答


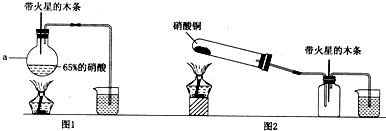


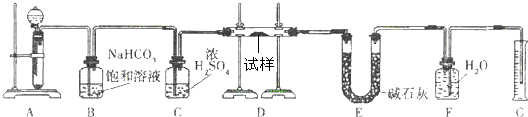

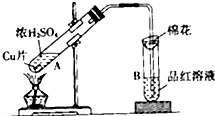 某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.