题目内容
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列两种不同的实验方案进行探究.请回答下列问题:
(一)甲组:
实验原理:镁铝合金
测定剩余固体质量
实验步骤:
①称量 用托盘天平称取2.7g镁铝合金粉末;
②溶解 把中药品加入烧杯中,用规格为 mL的量筒量取一定体积1.25mol/L NaOH溶液加入烧杯中,不断搅拌,充分反应:
③过滤;
④洗涤 若未对过滤所得不溶物进行洗涤,测得铝得质量分数将 (填“偏高”、“偏低”或“不变”),证明不溶物已洗涤干净得方法为
⑤干燥、称量剩余固体
(二)乙组:
实验原理:用等量的镁铝合金进行下述实验:
镁铝合金
测定生成气体的体积
镁铝合金
测定生成气体的体积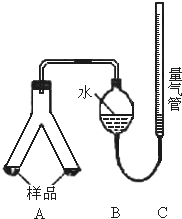
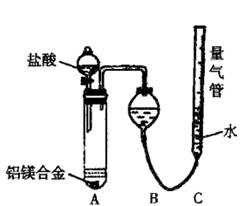
实验装置:如图.
实验步骤:
①按图连接好装置;
②称取两份质量相等的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,连接好A、B、C,然后调节C的高度使B和C中液面相平,记录下此时量气管液面读数为10mL;
③用注射器向装置A左侧管中注入足量的稀盐酸,待不再有气泡产生时,调节装置C的高度,使B和C中的液面相平,记录下此时量气管液面读数为25mL;
④用另一注射器向装置A右侧管中注入足量的NaOH溶液,待不再有气泡产生时,调节装置C的高度,使B和C中的液面相平,记录下此时量气管液面读数为35mL.
问题和讨论:
(1)上述实验步骤①和②之间必须加一步 的操作,具体方法为 .
(2)为使测定结果尽可能准确,实验中还应注意的问题是 .
(3)步骤③和步骤④中产生气体的体积比为 ,合金中铝的质量分数为 .
(一)甲组:
实验原理:镁铝合金
| 足量NaOH溶液 |
实验步骤:
①称量 用托盘天平称取2.7g镁铝合金粉末;
②溶解 把中药品加入烧杯中,用规格为
③过滤;
④洗涤 若未对过滤所得不溶物进行洗涤,测得铝得质量分数将
⑤干燥、称量剩余固体
(二)乙组:
实验原理:用等量的镁铝合金进行下述实验:
镁铝合金
| 足量稀盐酸 |
镁铝合金
| 足量NaOH溶液 |

实验装置:如图.
实验步骤:
①按图连接好装置;
②称取两份质量相等的镁铝合金样品粉末,分别放入A装置左右两个管中,向B装置中加入一定量的水,连接好A、B、C,然后调节C的高度使B和C中液面相平,记录下此时量气管液面读数为10mL;
③用注射器向装置A左侧管中注入足量的稀盐酸,待不再有气泡产生时,调节装置C的高度,使B和C中的液面相平,记录下此时量气管液面读数为25mL;
④用另一注射器向装置A右侧管中注入足量的NaOH溶液,待不再有气泡产生时,调节装置C的高度,使B和C中的液面相平,记录下此时量气管液面读数为35mL.
问题和讨论:
(1)上述实验步骤①和②之间必须加一步
(2)为使测定结果尽可能准确,实验中还应注意的问题是
(3)步骤③和步骤④中产生气体的体积比为
分析:(一)甲组②依据铝和氢氧化钠反应的化学方程式计算需要的氢氧化钠溶液体积,依据溶液体积选择量筒;
④固体表面沾有偏铝酸钠溶液,称量剩余固体质量会偏大,测定铝的质量分数减小;证明固体洗涤干净的方法是验证是否存在偏铝酸钠 溶液设计实验验证;
(二)乙组
(1)分析流程和步骤可知测定气体体积的方法测定合金质量分数,装置需要气密性完好,应对装置进行气密性检查;检查装置气密性的方法是利用装置中 压强变化和液面变化设计;
(2)使B和C中的液面相平,后还需要冷却溶液温度到室温读取气体体积;
(3)分析实验过程可知开始量气管是10ml,加入足量盐酸,镁和铝全部反应生成氢气,此时量气管体积为25ml,说明生成氢气为15ml;另一端加入氢氧化钠溶液和铝反应生成氢气,最后量气管读数为35ml,说明生成氢气体积为10ml;依据数据和反应生成氢气的量计算合金中铝的质量分数;
④固体表面沾有偏铝酸钠溶液,称量剩余固体质量会偏大,测定铝的质量分数减小;证明固体洗涤干净的方法是验证是否存在偏铝酸钠 溶液设计实验验证;
(二)乙组
(1)分析流程和步骤可知测定气体体积的方法测定合金质量分数,装置需要气密性完好,应对装置进行气密性检查;检查装置气密性的方法是利用装置中 压强变化和液面变化设计;
(2)使B和C中的液面相平,后还需要冷却溶液温度到室温读取气体体积;
(3)分析实验过程可知开始量气管是10ml,加入足量盐酸,镁和铝全部反应生成氢气,此时量气管体积为25ml,说明生成氢气为15ml;另一端加入氢氧化钠溶液和铝反应生成氢气,最后量气管读数为35ml,说明生成氢气体积为10ml;依据数据和反应生成氢气的量计算合金中铝的质量分数;
解答:解:(一)甲组:
②依据化学方程式计算,2Al+2NaOH+2H2O=2NaAlO2+H2↑,2.7g镁铝合金全部是铝的质量,物质的量为0.1mol,需要氢氧化钠物质的量0.1mol,所以氢氧化钠溶液体积=
=0.08L=80ml,依据选择量筒的原则是大而近,应选择100ml的量筒;
故答案为:100;
④固体表面沾有偏铝酸钠溶液,称量剩余固体质量会偏大,测定铝的质量分数减小,测定质量分数偏低;证明固体洗涤干净的方法是验证是否存在偏铝酸钠溶液设计实验验证,实验设计为:取少量洗涤液逐滴加入稀盐酸至过量,若整个过程未出现沉淀则说明洗涤干净;
故答案为:偏低,取少量洗涤液逐滴加入稀盐酸至过量,若整个过程未出现沉淀则说明洗涤干净;
(二)乙组
(1)分析流程和步骤可知测定气体体积的方法测定合金质量分数,装置需要气密性完好,应对装置进行气密性检查;检查方法为:向C中加入一定量水,然后提高C使其中液面高于B,静置一会儿,若液面不发生变化则气密性良好;
故答案为;检查气密性,向C中加入一定量水,然后提高C使其中液面高于B,静置一会儿,若液面不发生变化则气密性良好;
(2)使B和C中的液面相平,后还需要冷却溶液温度到室温读取气体体积,避免热溶液对读数产生误差;
故答案为:用量气管量气前气体是否冷却到室温;
(3)分析实验过程可知开始量气管是10ml,加入足量盐酸,镁和铝全部反应生成氢气,此时量气管体积为25ml,说明生成氢气为15ml;另一端加入氢氧化钠溶液和铝反应生成氢气,最后量气管读数为35ml,说明生成氢气体积为10ml,得到步骤③和步骤④中产生气体的体积比为15:10=3;2;依据化学方程式计算铝的质量分数,设合金中 镁物质的量为x,铝物质的量为y:
Mg+2HCl=MgCl2+H2↑,
1 1
x x
2Al+6HCl=2AlCl3+3H2↑,
2 3
y 1.5y
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
2 3
y 1.5y
x+1.5y=15
1.5y=10
x=5 mol
y=6.7mol
铝的质量分数=
×100%=60%
故答案为:3:2,60%;
②依据化学方程式计算,2Al+2NaOH+2H2O=2NaAlO2+H2↑,2.7g镁铝合金全部是铝的质量,物质的量为0.1mol,需要氢氧化钠物质的量0.1mol,所以氢氧化钠溶液体积=
| 0.1mol |
| 1.25mol/L |
故答案为:100;
④固体表面沾有偏铝酸钠溶液,称量剩余固体质量会偏大,测定铝的质量分数减小,测定质量分数偏低;证明固体洗涤干净的方法是验证是否存在偏铝酸钠溶液设计实验验证,实验设计为:取少量洗涤液逐滴加入稀盐酸至过量,若整个过程未出现沉淀则说明洗涤干净;
故答案为:偏低,取少量洗涤液逐滴加入稀盐酸至过量,若整个过程未出现沉淀则说明洗涤干净;
(二)乙组
(1)分析流程和步骤可知测定气体体积的方法测定合金质量分数,装置需要气密性完好,应对装置进行气密性检查;检查方法为:向C中加入一定量水,然后提高C使其中液面高于B,静置一会儿,若液面不发生变化则气密性良好;
故答案为;检查气密性,向C中加入一定量水,然后提高C使其中液面高于B,静置一会儿,若液面不发生变化则气密性良好;
(2)使B和C中的液面相平,后还需要冷却溶液温度到室温读取气体体积,避免热溶液对读数产生误差;
故答案为:用量气管量气前气体是否冷却到室温;
(3)分析实验过程可知开始量气管是10ml,加入足量盐酸,镁和铝全部反应生成氢气,此时量气管体积为25ml,说明生成氢气为15ml;另一端加入氢氧化钠溶液和铝反应生成氢气,最后量气管读数为35ml,说明生成氢气体积为10ml,得到步骤③和步骤④中产生气体的体积比为15:10=3;2;依据化学方程式计算铝的质量分数,设合金中 镁物质的量为x,铝物质的量为y:
Mg+2HCl=MgCl2+H2↑,
1 1
x x
2Al+6HCl=2AlCl3+3H2↑,
2 3
y 1.5y
2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
2 3
y 1.5y
x+1.5y=15
1.5y=10
x=5 mol
y=6.7mol
铝的质量分数=
| 6.7mol×27g/mol |
| 6.7mol×27g/mol+5mol×24g/mol |
故答案为:3:2,60%;
点评:本题考查了实验探究物质组成的实验设计和过程分析判断,掌握基础和 实验基本操作是关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 (一)甲组:实验方案:镁铝合金
(一)甲组:实验方案:镁铝合金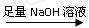 测定剩余固体质量
测定剩余固体质量 盘天平称量一定质量镁铝合金粉末
盘天平称量一定质量镁铝合金粉末 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积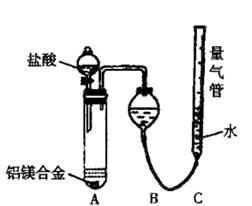

 并最终得到固体物质1.45g。则该合金中铝的质量分数为 。
并最终得到固体物质1.45g。则该合金中铝的质量分数为 。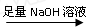 测定剩余固体质量
测定剩余固体质量 (二)乙组:实验方案:镁铝合金
(二)乙组:实验方案:镁铝合金 测定生成气体的体积
测定生成气体的体积