 等质量的铝粉与足量盐酸在不同条件下反应,产生H2的体积与反应时间关系如图所示,则图中曲线a、b、c分别对应表中的实验组别是( ) 等质量的铝粉与足量盐酸在不同条件下反应,产生H2的体积与反应时间关系如图所示,则图中曲线a、b、c分别对应表中的实验组别是( )
|
反应2SO2+O2?2SO3,5s内SO3的浓度增加了0.4mol/L,则在这段时间内用O2表示的反应速率(mol/L?s)为( )
| A、0.1 | B、0.08 | C、0.04 | D、0.02 |
对于反应2SO2(g)+O2(g)?2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是( )
(0~t1:v(正)=v(逆);t1时改变条件,t2时重新建立平衡)
(0~t1:v(正)=v(逆);t1时改变条件,t2时重新建立平衡)
A、 增加氧气的浓度 | B、 增大压强 | C、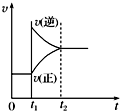 升高温度 | D、 加入催化剂 |
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g)?PCl5(g).5min末达到平衡,有关数据如下表:
|
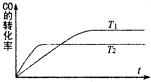 一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )
一定条件下,固定容积的密闭容器中,CO和H2反应生成甲醇:CO(g)+2H2(g)?CH3OH(g).如图是该反应在不同温度下CO的转化率随时间变化的曲线.下列判断正确的是( )| A、T1>T2 | B、该反应的△H>0 | C、T1时的平衡常数K1>T2时的平衡常数K2 | D、T1时的平衡常数K1<T2时的平衡常数K2 |
下列反应不存在化学反应限度的是( )
| A、合成氨反应 | B、氢氯爆鸣反应 | C、SO2的催化氧化反应 | D、氯气溶于水生成盐酸和次氯酸 |
从下列叙述中能肯定判断某化学平衡发生移动的是( )
| A、混合物中各组分的浓度改变 | B、混合体系中气体密度发生变化 | C、正、逆反应速率改变 | D、反应物的转化率改变 |
 已知(HF)2(g)?2HF(g),△H>0且平衡体系的总质量【m(总)】与总物质的量【n总】之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )
已知(HF)2(g)?2HF(g),△H>0且平衡体系的总质量【m(总)】与总物质的量【n总】之比在不同温度下随压强的变化曲线如图所示.下列说法正确的是( )| A、温度:T1<T2 | ||
| B、平衡常数:K(a)=K(b)<K(c) | ||
| C、反应速率:Vb>Va | ||
D、当
|
大气中的SO2是造成酸雨的主要污染物.最新研究表明,[N(CH3)4]2SO4(s)能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂[N(CH3)4]2SO4(s)+SO2(g)?[N(CH3)4]2S2O6(s)△H<0则用[N(CH3)4]2SO4(s)吸收SO2的适宜条件为( )
| A、高温高压 | B、低温高压 | C、高温低压 | D、低温低压 |