题目内容
对于反应2SO2(g)+O2(g)?2SO3(g)△H<0已达平衡,如果其他条件不变时,分别改变下列条件,对化学反应速率和化学平衡产生影响,下列条件与图象不相符的是( )
(0~t1:v(正)=v(逆);t1时改变条件,t2时重新建立平衡)
(0~t1:v(正)=v(逆);t1时改变条件,t2时重新建立平衡)
A、 增加氧气的浓度 | B、 增大压强 | C、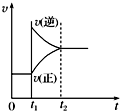 升高温度 | D、 加入催化剂 |
分析:A、增大反应物的浓度,化学反应速率加快,化学平衡向着正反应方向进行;
B、增大压强,正逆反应速率都加快,化学平衡向着气体体积减小的方向进行;
C、升高温度,化学反应速率加快,化学平衡向着吸热方向进行;
D、加入催化剂,化学反应速率加快,化学平衡不移动.
B、增大压强,正逆反应速率都加快,化学平衡向着气体体积减小的方向进行;
C、升高温度,化学反应速率加快,化学平衡向着吸热方向进行;
D、加入催化剂,化学反应速率加快,化学平衡不移动.
解答:解:A、增大反应物氧气的浓度,正逆化学反应速率加快,化学平衡向着正反应方向进行,逆反应在原来基础上加快,正反应速率迅速加快,且快于逆反应速率,故A正确;
B、增大压强,此时正逆反应速率都迅速加快,化学平衡向着气体体积减小的方向即向着正方向进行,正反应速率快于逆反应速率,故B正确;
C、升高温度,化学反应速率都离开原来的速率点迅速加快,化学平衡向着吸热方向进行,即向着逆方向进行,逆反应速率快于正反应速率,故C错误;
D、加入催化剂,正逆化学反应速率同等程度的加快,化学平衡不移动,故D正确.
故选C.
B、增大压强,此时正逆反应速率都迅速加快,化学平衡向着气体体积减小的方向即向着正方向进行,正反应速率快于逆反应速率,故B正确;
C、升高温度,化学反应速率都离开原来的速率点迅速加快,化学平衡向着吸热方向进行,即向着逆方向进行,逆反应速率快于正反应速率,故C错误;
D、加入催化剂,正逆化学反应速率同等程度的加快,化学平衡不移动,故D正确.
故选C.
点评:本题考查学生影响化学反应速率化学平衡移动的因素致使,注意温度、压强对正逆反应速率的影响是离开原来平衡速率点的,难度不大.

练习册系列答案
相关题目
下列有关说法正确的是( )
| A、准确称取0.4000g NaOH固体可配成100mL 0.1000mol?L-1的NaOH标准溶液 | B、催化剂可以加快化学反应速率但不能改变化学反应的焓变 | C、100mL pH=3的HA和HB分别与足量的锌反应,HB放出的氢气多,说明HB酸性比HA弱 | D、对于反应2SO2(g)+O2(g)?2SO3(g),压缩气体体积使压强增大(其他条件不变),则SO2的转化率增大,平衡常数K也增大 |