(1)已知X、Y、Z为同一短周期的三种元素,其原子的部分电离能(kJ/mol)如下表所示:
①三种元素在周期表中位于第 周期
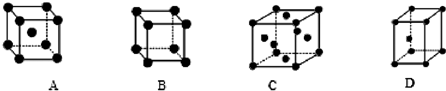
②X晶体采用的堆积方式是下列中 (填字母)
(2)已知N-N、N=N、N≡N键能之比为1.00:2.17:4.90,而C-C、C=C、C≡C键能之比为1.00:1.77:2.34,由此你得出的结论是 .
(3)N2O的等电子体为:①分子 ,②阴离子 ;由此可知N2O的中心原子的杂化类型为 .根据价层电子对互斥模型确定NO2的分子构型为 .
(4)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,请在图中标出水合铜离子中的配位键.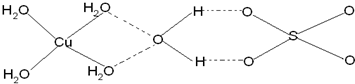
0 22159 22167 22173 22177 22183 22185 22189 22195 22197 22203 22209 22213 22215 22219 22225 22227 22233 22237 22239 22243 22245 22249 22251 22253 22254 22255 22257 22258 22259 22261 22263 22267 22269 22273 22275 22279 22285 22287 22293 22297 22299 22303 22309 22315 22317 22323 22327 22329 22335 22339 22345 22353 203614
| X | Y | Z | |
| I1 | 496 | 738 | 577 |
| I2 | 4562 | 1451 | 1817 |
| I3 | 6912 | 7733 | 2754 |
| I4 | 9540 | 10540 | 11578 |
②X晶体采用的堆积方式是下列中

(2)已知N-N、N=N、N≡N键能之比为1.00:2.17:4.90,而C-C、C=C、C≡C键能之比为1.00:1.77:2.34,由此你得出的结论是
(3)N2O的等电子体为:①分子
(4)已知铜能形成多种化合物,如硫酸铜的结构如下图所示,请在图中标出水合铜离子中的配位键.
